Resumen de los puntos importantes del artículo sobre Steatotic Liver Disease (SLD)
- Nueva Nomenclatura y Clasificación:
- NAFLD ahora se denomina Metabolic Dysfunction-Associated Steatotic Liver Disease (MASLD).
- Se incluyen nuevas categorías: MetALD (combinación de MASLD y ALD) y ALD (Alcohol-Related Liver Disease).
- Reemplazo del término «fatty liver» por «steatotic liver» para reducir estigma.
- Epidemiología y Factores de Riesgo:
- Afecta al 30% de la población mundial.
- Factores principales: obesidad, resistencia a la insulina y consumo de alcohol.
- La fibrosis hepática es el principal predictor de mortalidad.
- Diagnóstico y Evaluación:
- Se recomienda un enfoque escalonado con pruebas no invasivas como FIB-4 y elastografía.
- La detección temprana de fibrosis avanzada es clave para el manejo.
- Tratamiento y Manejo:
- Pérdida de peso del 7-10% mejora la fibrosis.
- Tratamientos farmacológicos en estudio incluyen GLP-1 agonistas (semaglutida), agonistas PPAR y FGF21.
- Para ALD, la reducción o abstinencia del alcohol mejora el pronóstico.
- Prognosis y Seguimiento:
- Riesgo progresivo de cirrosis y descompensación hepática en MASLD, MetALD y ALD.
- Estrategias de monitoreo deben enfocarse en fibrosis y factores cardiometabólicos.
- Futuro y Desarrollo de Terapias:
- Resmetirom es el primer fármaco aprobado para MASLD con fibrosis avanzada.
- En estudios, GLP-1 y FGF21 muestran potencial en la reducción del consumo de alcohol y la progresión hepática.
- Resmetirom es el primer fármaco aprobado para MASLD con fibrosis avanzada.

Panel 1: Esteatosis hepática y enfermedad hepática crónica
La esteatosis hepática se define como la acumulación de lípidos en las células parenquimatosas del hígado. El consumo de alcohol ha sido reconocido desde hace tiempo como una causa de esteatosis hepática; sin embargo, existen informes de casos de esteatosis hepática en personas que no consumen alcohol, que datan desde el siglo XIX, y algunos de estos informes ya relacionaban la enfermedad con la obesidad y la diabetes.
En 1980, Ludwig y sus colegas describieron una serie de pacientes con esteatosis hepática que no consumían alcohol y propusieron el término enfermedad del hígado graso no alcohólica (NAFLD, por sus siglas en inglés) para diferenciarla de la causa bien conocida del daño hepático inducido por el alcohol. Desde entonces, la NAFLD ha sido vinculada con la disfunción metabólica, caracterizada principalmente por obesidad y diabetes.
En 2023, la NAFLD fue redefinida e integrada en el espectro de la enfermedad hepática esteatósica (steatotic liver disease) a partir de un proceso de consenso global, el cual ahora es respaldado por más de 75 sociedades en todo el mundo.
La relevancia clínica de la esteatosis hepática sigue siendo debatida; sin embargo, los factores que contribuyen a la esteatosis (obesidad, diabetes y alcohol) también pueden desencadenar inflamación hepática y fibrosis. Con el tiempo, la progresión de la fibrosis hepática puede llevar a cirrosis y sus complicaciones, asociadas con una alta mortalidad.
Por lo tanto, la detección de la fibrosis hepática, más que la esteatosis en sí, es la piedra angular de la mayoría de las iniciativas destinadas a identificar, intervenir y prevenir la enfermedad hepática esteatósica sintomática.

Panel 2: Prevalencia global de factores de riesgo para la enfermedad hepática esteatósica
- 43% tienen sobrepeso.
- 16% viven con obesidad.
- 6% tienen diabetes tipo 2.
- 50% consumen alcohol regularmente.
- 20% beben en exceso al menos una vez al mes.
- 16% tienen un consumo de alcohol perjudicial.
- 25% portan alelos de riesgo genético en PNPLA3.
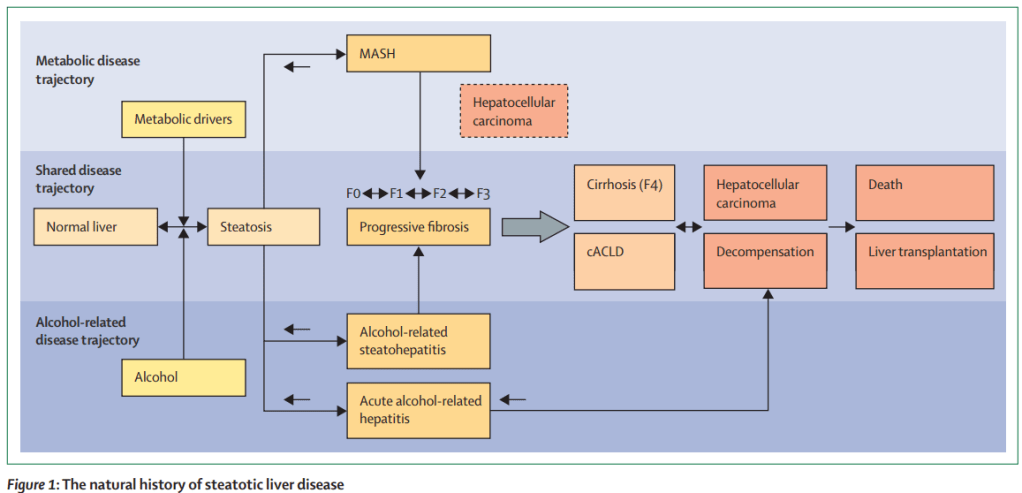
Figura 1: La historia natural de la enfermedad hepática esteatósica
Este diagrama muestra la progresión de la enfermedad hepática esteatósica a través de diferentes trayectorias:
- Trayectoria metabólica:
- Factores metabólicos llevan a la esteatosis hepática.
- Puede evolucionar a MASH (esteatohepatitis asociada a disfunción metabólica).
- Puede desarrollar carcinoma hepatocelular.
- Trayectoria compartida:
- Un hígado normal puede desarrollar esteatosis, que puede progresar a fibrosis hepática (F0 a F3).
- La fibrosis avanzada puede llevar a cirrosis (F4) y enfermedad hepática crónica avanzada compensada (cACLD).
- La cirrosis puede descompensarse, causando carcinoma hepatocelular, insuficiencia hepática y necesidad de trasplante.
- Trayectoria relacionada con el alcohol:
- El consumo de alcohol puede causar esteatohepatitis alcohólica o hepatitis alcohólica aguda.
- Ambas pueden acelerar la progresión a fibrosis, cirrosis y sus complicaciones.

Figura 2: Diagrama de flujo de clasificación y subclasificación de la enfermedad hepática esteatósica
Este diagrama muestra cómo se clasifica la enfermedad hepática esteatósica según la presencia de factores cardiometabólicos y el consumo de alcohol.
- Diagnóstico inicial:
- Se confirma la esteatosis hepática mediante histología o imágenes.
- Si no hay esteatosis visible, pero hay fibrosis avanzada y factores de riesgo, se presume la enfermedad hepática esteatósica.
- Evaluación de factores cardiometabólicos:
- Si hay al menos un factor de riesgo cardiometabólico (obesidad, diabetes, hipertensión, etc.), se cuantifica el consumo de alcohol.
- Clasificación según el consumo de alcohol:
- MASLD: Consumo de alcohol <20 g/día (mujeres) o <30 g/día (hombres).
- MetALD: Consumo de alcohol entre 20–50 g/día (mujeres) o 30–60 g/día (hombres).
- ALD: Consumo de alcohol >50 g/día (mujeres) o >60 g/día (hombres).
- Si no hay factores cardiometabólicos, se clasifica según el consumo de alcohol en ALD u otras causas de esteatosis hepática.
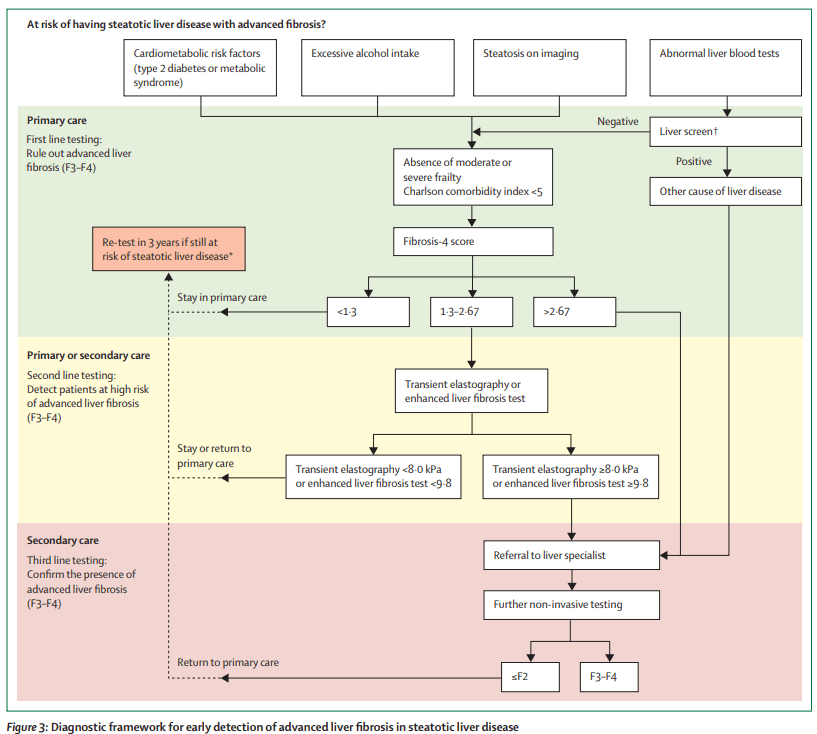
Figura 3: Marco de diagnóstico para la detección temprana de fibrosis hepática avanzada en la enfermedad hepática esteatósica
Este diagrama muestra un enfoque escalonado para identificar la fibrosis avanzada (F3-F4) en pacientes con enfermedad hepática esteatósica.
- Identificación de pacientes en riesgo:
- Factores de riesgo incluyen síndrome metabólico, consumo excesivo de alcohol, esteatosis en imágenes o alteraciones en pruebas hepáticas.
- Si las pruebas hepáticas anormales indican otra causa de enfermedad hepática, se sigue una ruta diferente.
- Atención primaria (primera línea):
- Se usa el puntaje Fibrosis-4 (FIB-4) para descartar fibrosis avanzada.
- Si FIB-4 es menor a 1.3, el paciente permanece en atención primaria y se recomienda repetir la prueba en 3 años si persiste el riesgo.
- Si FIB-4 es entre 1.3 y 2.67, se requiere una prueba adicional (elastografía transitoria o prueba de fibrosis hepática mejorada).
- Atención primaria/secundaria (segunda línea):
- Si la elastografía muestra valores <8.0 kPa o la prueba de fibrosis hepática es <9.8, el paciente regresa a atención primaria.
- Si los valores son ≥8.0 kPa o ≥9.8, el paciente se deriva a un especialista en hígado.
- Atención secundaria (tercera línea):
- Se realizan más pruebas no invasivas para confirmar fibrosis avanzada.
- Si el paciente tiene fibrosis avanzada (F3-F4), se maneja en atención especializada; si no, regresa a atención primaria.

Tabla 1: Biomarcadores más comunes para la evaluación de fibrosis y pronóstico en la enfermedad hepática esteatósica
Esta tabla compara diferentes biomarcadores utilizados para la detección de fibrosis avanzada y su capacidad predictiva para eventos hepáticos.
Puntos clave:
- Pruebas de primera línea:
- Fibrosis-4 (FIB-4): Fácil de calcular, útil para descartar fibrosis avanzada (F3-F4).
- LiverRisk Score: Derivado de la población general, su utilidad clínica aún está en evaluación.
- NAFLD Fibrosis Score: Menos preciso que FIB-4, pero válido en enfermedad esteatósica metabólica.
- Pruebas de segunda línea:
- Elastografía transitoria y 2D shear wave elastography: Métodos de imagen con buena precisión diagnóstica.
- Enhanced Liver Fibrosis (ELF) test: Basado en marcadores séricos, pero influenciado por la edad.
- ADAPT Score: Incluye Pro-C3 y parámetros metabólicos, pero requiere más validación.
- Prueba de tercera línea:
- Elastografía por resonancia magnética: Método con la mayor precisión diagnóstica (AUROC 0.92), pero de acceso limitado.
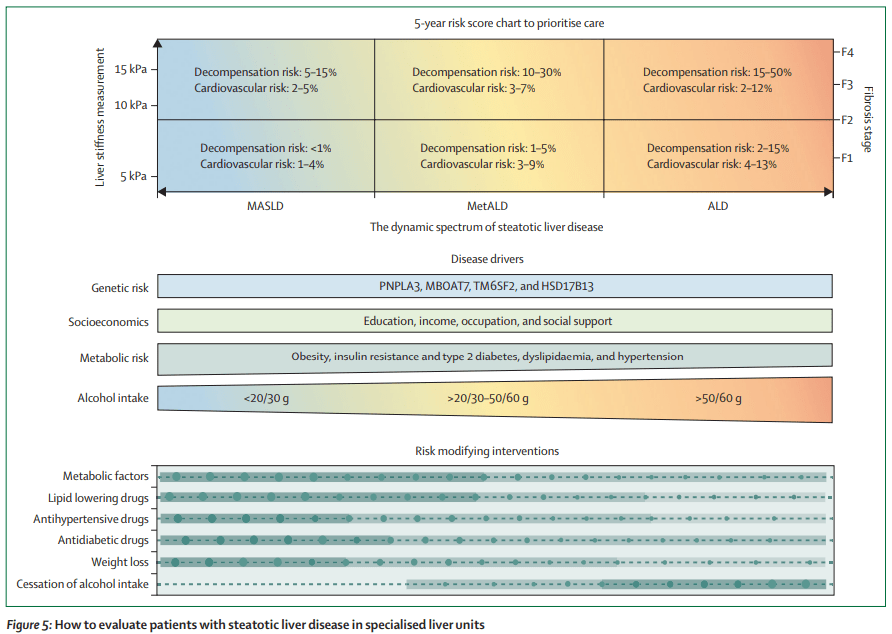
Figura 5: Evaluación de pacientes con enfermedad hepática esteatósica en unidades especializadas
Este diagrama muestra un enfoque para priorizar el manejo de la enfermedad hepática esteatósica según el riesgo de descompensación hepática y enfermedad cardiovascular en los próximos 5 años.
1. Evaluación del riesgo (según elastografía y fibrosis hepática)
- Medición de rigidez hepática (FibroScan):
- 5 kPa: Riesgo de descompensación <1%, riesgo cardiovascular 1-4%.
- 10 kPa: Riesgo de descompensación 1-5%, riesgo cardiovascular 3-9%.
- 15 kPa: Riesgo de descompensación 5-15%, riesgo cardiovascular 2-5%.
- Mayor severidad en MetALD y ALD: Riesgo de descompensación hasta 50%.
2. Factores de la enfermedad
- Riesgo genético: Variantes en PNPLA3, MBOAT7, TM6SF2 y HSD17B13.
- Factores socioeconómicos: Educación, ingresos, empleo y apoyo social.
- Factores metabólicos: Obesidad, resistencia a la insulina, dislipidemia e hipertensión.
- Consumo de alcohol: Se clasifica según la cantidad ingerida.
3. Intervenciones para modificar el riesgo
- Factores metabólicos: Manejo de obesidad y comorbilidades.
- Fármacos hipolipemiantes, antihipertensivos y antidiabéticos.
- Pérdida de peso y reducción del consumo de alcohol.

Panel 4: Tratamientos estándar para factores de riesgo cardiometabólicos y consumo de alcohol
- Sobrepeso u obesidad:
- Objetivo: pérdida de peso del 7-10% con un enfoque escalonado.
- Iniciar con consejería sobre estilo de vida, dieta y ejercicio.
- Considerar agonistas GLP-1, agonistas duales o cirugía bariátrica si las modificaciones del estilo de vida no son suficientes.
- Fármacos para bajar de peso en IMC >30 kg/m² o >35 kg/m² con comorbilidades.
- Cirugía bariátrica en IMC >40 kg/m² o >35 kg/m² con comorbilidades.
- Diabetes tipo 2:
- Preferencia por fármacos que impacten la inflamación o fibrosis hepática:
- Agonistas del receptor GLP-1.
- Inhibidores SGLT2.
- Pioglitazona.
- La elección depende del IMC y comorbilidades.
- Preferencia por fármacos que impacten la inflamación o fibrosis hepática:
- Hiperlipidemia:
- Uso de estatinas para prevención primaria o secundaria de eventos cardiovasculares según guías clínicas.
- Hipertensión:
- Iniciar tratamiento si la presión arterial es >140/90 mmHg, o >130/80 mmHg en diabéticos.
- No hay preferencia por una clase específica de fármacos.
- Tabaquismo:
- Se debe incentivar el cese del tabaquismo.
- Se puede ofrecer farmacoterapia si es necesario.
- Apnea del sueño:
- Evaluar a los pacientes y considerar presión positiva continua en la vía aérea (CPAP) si se requiere.
- Consumo de alcohol:
- Cualquier reducción mejora los resultados.
- En fibrosis avanzada o cirrosis, se recomienda abstinencia total.
- Se debe evitar el consumo excesivo en atracones (binge drinking).
- Se recomienda terapia conductual y medicamentos como acamprosato o naltrexona.
- Pacientes con trastorno por consumo de alcohol deben ser derivados a programas especializados.
Descubre más desde Medicina Cardiometabólica
Suscríbete y recibe las últimas entradas en tu correo electrónico.

