Introducción
La enfermedad por hígado graso no alcohólico (NAFLD), recientemente redefinida como enfermedad por esteatosis hepática asociada a disfunción metabólica (MASLD), constituye hoy la enfermedad hepática crónica más prevalente a nivel mundial, afectando a un 25-30% de la población. Su estrecha relación con la obesidad, diabetes tipo 2, dislipidemia e hipertensión arterial refleja su carácter multisistémico y cardiometabólico.
La transición del término “NAFLD” a “MASLD” en 2023 buscó enfatizar su origen metabólico y abandonar un criterio diagnóstico basado en la exclusión del consumo alcohólico.
Evolución patológica de MASLD
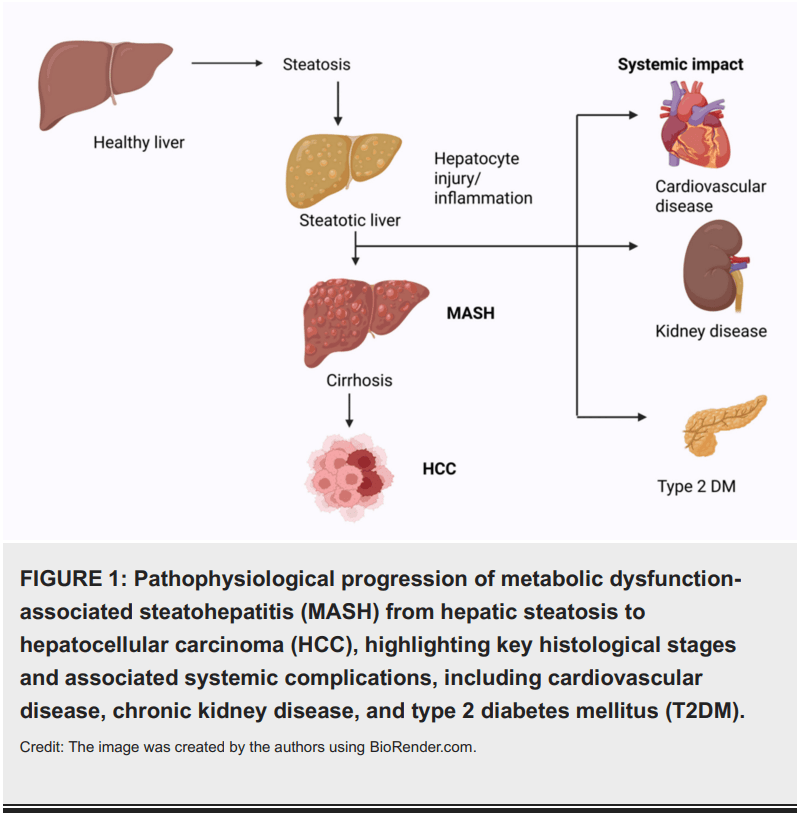
MASLD es un continuo progresivo que puede ir desde la esteatosis simple hasta la cirrosis y el carcinoma hepatocelular (HCC).
- Esteatosis simple: acumulación de triglicéridos en >5% de hepatocitos.
- MASH (esteatohepatitis asociada a disfunción metabólica): inflamación lobulillar, balonización hepatocitaria y fibrosis variable.
- Fibrosis hepática: la etapa histológica más predictiva de mortalidad.
- Cirrrosis y HCC: riesgo incluso sin cirrosis, lo que dificulta la vigilancia.
Mecanismos clave
- Resistencia a la insulina y lipotoxicidad.
- Estrés oxidativo y disfunción mitocondrial.
- Inflamación mediada por células inmunes (Kupffer, macrófagos, linfocitos).
- Eje intestino-hígado: disbiosis y permeabilidad intestinal aumentada.
- Genética: variantes como PNPLA3, TM6SF2, MBOAT7 aumentan el riesgo; HSD17B13 puede ser protector.
- Epigenética: microARN (miR-122, miR-34a, miR-192) como biomarcadores emergentes.
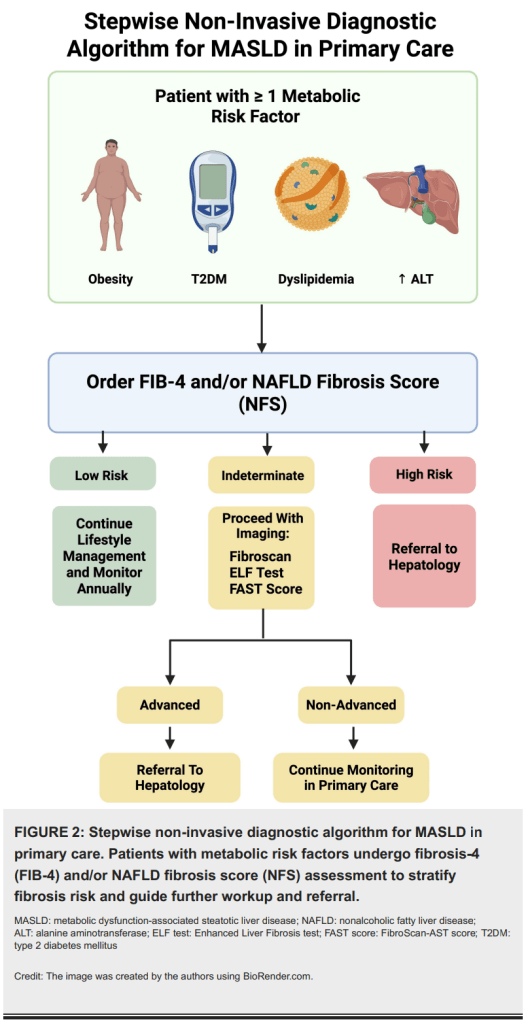
Herramientas diagnósticas no invasivas
El biopsia hepática sigue siendo el estándar de oro, pero está siendo desplazada por métodos no invasivos:
- Scores séricos:
- FIB-4 (edad, AST, ALT, plaquetas).
- NAFLD Fibrosis Score (incluye IMC, diabetes, albúmina).
- ELF test (ácido hialurónico, TIMP-1, PIIINP).
- Imágenes:
- Ecografía abdominal (útil pero limitada).
- Elastografía transitoria (FibroScan): mide rigidez hepática y esteatosis (CAP).
- MRI-PDFF y MRE: mayor precisión en cuantificación de grasa y fibrosis.
Estrategias de manejo en Medicina Interna
1. Modificaciones del estilo de vida – pilar del tratamiento
- Pérdida de peso ≥7%: mejora histología; ≥10% puede revertir NASH y fibrosis.
- Ejercicio aeróbico y de resistencia: 150–300 min/semana.
- Dieta mediterránea: beneficios metabólicos y hepáticos.
2. Terapias farmacológicas
Actualmente, no hay fármacos aprobados específicamente, pero destacan:
- Pioglitazona: mejora histología en diabéticos (limitada por efectos adversos).
- Vitamina E: beneficios en no diabéticos, riesgo de seguridad a largo plazo.
- GLP-1 RAs (liraglutida, semaglutida): reducción de grasa hepática y resolución de NASH.
- SGLT2-i: mejoran glucemia y reducen grasa hepática.
- Resmetirom (THR-β agonista) y obetichólico (FXR agonista): en fase avanzada de investigación.
3. Cirugía bariátrica
- Indicada en obesidad severa con NASH refractario.
- Demuestra mejoría histológica en hasta 85% de pacientes.
4. Manejo de factores de riesgo cardiometabólico
- Diabetes: preferir GLP-1 RA y SGLT2-i.
- Dislipidemia: estatinas seguras y eficaces.
- Hipertensión: RAAS bloqueadores con posible efecto antifibrótico.
- Riesgo cardiovascular: estratificación, aspirina cuando indicada, cesación tabáquica.
Biomarcadores y terapias emergentes
- CK-18, FAST score, exosomas y microARN como nuevas herramientas diagnósticas.
- FGF21 análogos (pegozafermin, efruxifermin): mejoran grasa hepática y sensibilidad insulínica.
- Lanifibranor (pan-PPAR), inhibidores ACC y SCD-1, y combinaciones (ej. tirzepatida GLP-1/GIP) muestran resultados prometedores.

Implicaciones clínicas y de política sanitaria
- El cambio a MASLD implica una visión más inclusiva y proactiva en el diagnóstico.
- El USPSTF aún no recomienda tamizaje poblacional, pero las sociedades (AASLD, ADA, EASL) sugieren evaluar fibrosis en pacientes con factores de riesgo metabólico.
- Integrar calculadoras de FIB-4 en historia clínica electrónica y facilitar acceso a elastografía es clave.
- Se requieren políticas públicas que incluyan a MASLD en los programas nacionales de salud hepática y cardiometabólica.
Conclusiones
MASLD es más que una enfermedad hepática: es un síndrome cardiometabólico multisistémico. La detección temprana mediante herramientas no invasivas, el manejo integral de factores de riesgo, y la adopción de estilos de vida saludables son esenciales.
La investigación en fármacos, biomarcadores, inteligencia artificial y multi-ómica anuncia un futuro de medicina personalizada en hepatología.
La integración de hepatología, endocrinología, cardiología, nefrología y atención primaria será fundamental para mejorar resultados y reducir la carga poblacional de MASLD.
Dr. Jorge Rojas, Médico Internista
Certificado en Salud Cardiometabólica – CMHC (USA)
- 🎧 Podcast: Medicina Cardiometabólica en Spotify
- 📸 Instagram: @drjorgerojas
- 👨🏫 Grupo de Facebook: Medicina Interna – Comunidad Académica
- 💬 Canal de WhatsApp: Únete aquí
- 📨 Canal de Messenger (Facebook): Únete aquí
- 📲 Canal de Instagram: Únete aquí

Suscríbete para seguir leyendo
Suscríbete para obtener acceso al contenido íntegro de esta entrada y demás contenido exclusivo para suscriptores.

