La coexistencia de enfermedad renal crónica (ERC) e insuficiencia cardíaca (IC) constituye una de las mayores intersecciones clínicas de la medicina actual. El síndrome cardiorrenal combina fisiopatologías superpuestas, aumenta el riesgo de hospitalización y muerte, y desafía la eficacia de los tratamientos tradicionales. Este documento expande en profundidad los puntos clave del artículo de revisión más reciente (CKJ, 2025).
1. Fisiopatología de la congestión en IC + ERC
- La cascada de congestión:
- Congestión hemodinámica: incremento de la presión telediastólica ventricular izquierda y de la presión capilar pulmonar.
- Fase intermedia asintomática: detectable por biomarcadores (BNP/NT-proBNP) o imagen (ecografía pulmonar: líneas B; Rx: Kerley B).
- Congestión clínica: edema pulmonar manifiesto, disnea, ortopnea, ganancia de peso, estertores húmedos.
- Particularidades en ERC:
- En ERC estadio 5D (hemodiálisis) la alternancia entre acumulación de líquidos y ultrafiltración brusca genera un ciclo de sobrecarga-depleción.
- La sobrecarga de volumen medida objetivamente (US, bioimpedancia) es el predictor más potente de mortalidad, superando a factores clásicos (HTA, diabetes).
2. Restricción de sodio y líquidos: ¿hasta dónde?
- Guías ESC 2024: sodio ≤2 g/día y líquidos 1.5–2 L/día, pero solo en subgrupos.
- Guías KDIGO 2024: sodio <2 g/día, principalmente para control de hipertensión.
- Evidencia CRIC: el riesgo cardiovascular se estabiliza con ~3 g/día de NaCl → un objetivo más práctico y alcanzable.
- Ensayo Herrmann 2025 (Nature Medicine): no diferencias en calidad de vida entre restricción hídrica vs consumo liberal; restricción sí aumentó sensación de sed.
Mensaje clínico:
- Evitar restricciones universales y estrictas.
- Personalizar metas para optimizar adherencia y prevenir hiponatremia o deshidratación.
3. Estrategias farmacológicas de decongestión
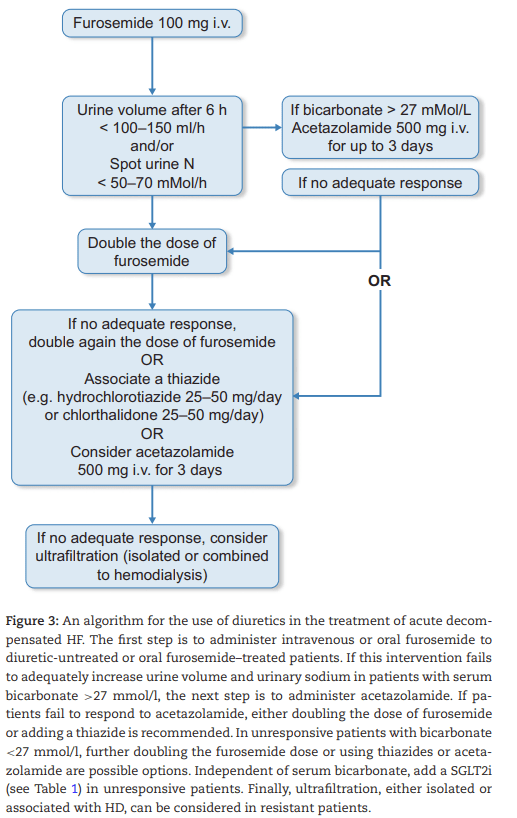
3.1. Diuréticos de asa: primera línea
- Furosemida, bumetanida: pilar inicial en IC aguda y crónica.
- Limitaciones: resistencia diurética y respuesta variable en ERC avanzada.
3.2. Combinación secuencial de nefronas
- Tiazidas (clortalidona, metolazona, hidroclorotiazida): útiles incluso en ERC avanzada, aunque antes se consideraban ineficaces.
- Acetazolamida: bloquea respuesta compensatoria proximal → incrementa descongestión (ADVOR trial: 42% éxito vs 31%).
- Triple combinación (asa + tiazida + acetazolamida): estrategia potente en resistencia diurética.
3.3. MRAs (espironolactona, eplerenona, finerenona)
- Reducen congestión y NT-proBNP.
- Finerenona: menos riesgo de hiperK, mostró beneficio en IC con FE preservada o levemente reducida.
- Limitación: falta de ensayos en IC aguda descompensada.
3.4. SGLT2i (dapagliflozina, empagliflozina)
- Mecanismo: osmótica + natriurética, ↓ precarga, ↓ consumo de O₂, cambio metabólico a cetonas.
- Beneficios:
- En IC aguda: seguros, ↑ diuresis, ↓ duración de terapia i.v.
- En IC crónica: ↓ hospitalizaciones, mejoría de síntomas.
- Limitaciones: no indicados en diálisis; inicio contraindicado con eGFR <20.
3.5. Tolvaptan (antagonista de vasopresina V2)
- ↑ excreción de agua libre, útil en hiponatremia.
- Evidencia conflictiva: mejora síntomas, pero no mortalidad ni rehospitalización.
- Riesgo: deterioro renal y costo elevado.
3.6. Ultrafiltración
- Permite extracción de volumen isotónico de forma controlada.
- Ensayo CARRESS-HF: inferior a tratamiento farmacológico (↑ creatinina, más eventos adversos).
- Recomendación: solo en casos refractarios y centros especializados.
3.7. Estrategias adyuvantes
- Solución salina hipertónica (3%): ↑ eficacia diurética, mejora alteraciones metabólicas, pero falta evidencia sólida.
- Terapias continuas (CVVH): reservadas para críticos con IC + fracaso renal que no toleran hemodiálisis convencional.
4. Monitoreo de la descongestión
- BNP/NT-proBNP: pueden guiar terapia, aunque la evidencia es heterogénea.
- Ecografía pulmonar: estrategias guiadas reducen rehospitalización y eventos cardiovasculares.
- Bioimpedancia y peso seco en diálisis: permiten ajustes finos.
- PROs (Patient-Reported Outcomes): calidad de vida, disnea y fatiga deben considerarse desenlaces primarios.
5. Diferencias entre guías internacionales
- ESC 2021/2024: recomiendan ecografía pulmonar y NT-proBNP para monitorizar congestión.
- AHA/ACC/HFSA 2022: menos énfasis en imagen, priorizan estrategias farmacológicas secuenciales.
- KDIGO 2024: foco en control de sodio y HTA, reconociendo limitaciones de restricción estricta.
6. Perspectivas futuras
- Ensayos clínicos de SGLT2i y MRAs en pacientes dializados.
- Validación del rol de finerenona en IC aguda con FE reducida.
- Incorporación de tecnologías de monitoreo continuo de volumen (sensores implantables, bioimpedancia portátil).
- Inclusión sistemática de PROs en ensayos de IC + ERC.
- Desarrollo de algoritmos personalizados integrando biomarcadores, imagen y clínica.
7. Resumen práctico para el clínico
- La congestión es el principal factor pronóstico en IC + ERC.
- Restricciones moderadas de sodio (~3 g/día) son más prácticas y seguras.
- La resistencia diurética debe enfrentarse con secuencialidad farmacológica.
- SGLT2i y MRAs aportan beneficios renocardiometabólicos adicionales.
- Ultrafiltración se reserva a refractarios en centros con experiencia.
- Ecografía pulmonar y BNP permiten detección y seguimiento precoz.
- El manejo debe ser integral, personalizado y centrado en calidad de vida.
Conclusión
El tratamiento de la congestión en pacientes con IC y ERC avanzada exige una estrategia multimodal y personalizada. Los avances farmacológicos (SGLT2i, acetazolamida, finerenona) junto con herramientas de monitorización (ecografía pulmonar, biomarcadores) marcan un nuevo paradigma. Sin embargo, persisten vacíos de evidencia en población dialítica y en IC con fracción de eyección preservada. El futuro deberá integrar innovación terapéutica, medicina personalizada y tecnología para mejorar desenlaces clínicos y calidad de vida en este grupo de altísimo riesgo.
Dr. Jorge Rojas, Médico Internista
Certificado en Salud Cardiometabólica – CMHC (USA)
Enfoque clínico en enfermedades cardiometabólicas, prevención y manejo integral del paciente crónico.
📲 ¿Quieres seguir aprendiendo sobre salud cardiometabólica?
Te invito a explorar mis contenidos y participar de esta comunidad profesional:
- 🎧 Podcast: Medicina Cardiometabólica en Spotify
- 📸 Instagram: @drjorgerojas
- 👨🏫 Grupo de Facebook: Medicina Interna – Comunidad Académica
- 💬 Canal de WhatsApp: Únete aquí
- 📨 Canal de Messenger (Facebook): Únete aquí
- 📲 Canal de Instagram: Únete aquí

Suscríbete para seguir leyendo
Suscríbete para obtener acceso al contenido íntegro de esta entrada y demás contenido exclusivo para suscriptores.

