1. Introducción y justificación del consenso
El uso de terapias antitrombóticas (anticoagulantes y antiagregantes) ha aumentado de forma exponencial en las últimas décadas, impulsado por el envejecimiento poblacional, la alta prevalencia de fibrilación auricular, enfermedad cardiovascular ateroesclerótica y la expansión de procedimientos intervencionistas. Se estima que más de 6 millones de pacientes en Europa bajo tratamiento antitrombótico se someten anualmente a procedimientos invasivos.
Aunque existía un consenso previo (2018), su baja adherencia en la práctica clínica se asoció a un aumento significativo tanto de eventos trombóticos como hemorrágicos. Este documento 2025 surge con el objetivo de:
- Simplificar la toma de decisiones.
- Homogeneizar la práctica clínica entre especialidades.
- Incorporar nueva evidencia (DOAC, DAPT abreviada, reversores específicos).
- Reducir eventos adversos prevenibles.
El consenso está respaldado por más de 25 sociedades científicas, lo que refuerza su aplicabilidad transversal.
2. Evaluación del riesgo tromboembólico
2.1. Pacientes en tratamiento anticoagulante
El riesgo tromboembólico incluye:
- Eventos arteriales: ictus, embolia sistémica (FA, prótesis valvulares).
- Eventos venosos: recurrencia de TVP/TEP.
El documento propone una estratificación binaria práctica:
- Riesgo bajo–intermedio: ≤10% anual.
- Riesgo alto: >10% anual.
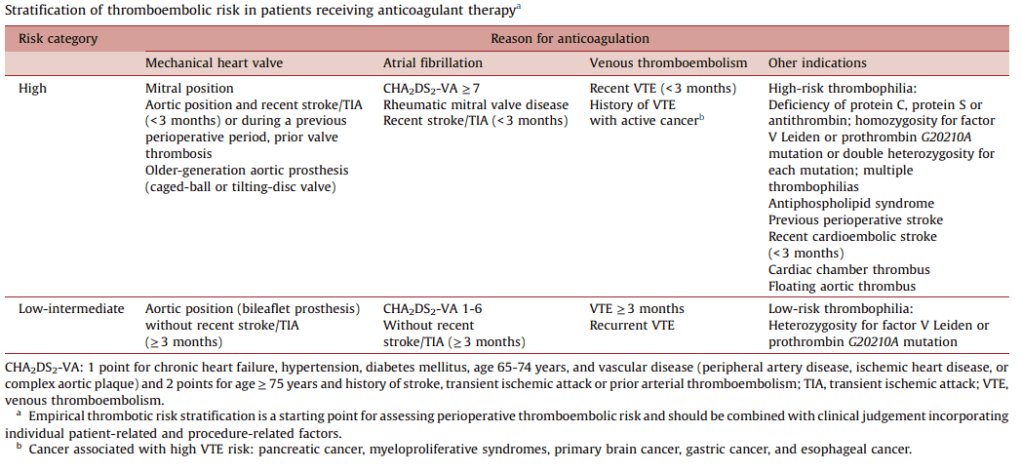
Se actualiza el uso del CHA₂DS₂-VA (sin sexo femenino como factor independiente), alineado con guías ESC 2024.
Son considerados alto riesgo:
- FA con CHA₂DS₂-VA ≥7.
- Ictus/TEP reciente (<3 meses).
- Prótesis valvulares mecánicas de alto riesgo.
- Trombofilias mayores o síndrome antifosfolípido.
- Trombo intracardíaco o aórtico flotante.
👉 Esta estratificación es clave para decidir si se justifica terapia puente con heparina, que queda restringida a escenarios muy seleccionados.
2.2. Pacientes en tratamiento antiagregante
El riesgo trombótico depende fundamentalmente del tiempo desde el evento isquémico o revascularización:
- Riesgo máximo:
- Primeras 4–6 semanas post-PCI.
- Primer mes post-SCA o ictus isquémico.
- Riesgo intermedio:
- Hasta 6 meses (PCI estable).
- Riesgo bajo:
- 6–12 meses, según contexto clínico.
Factores que aumentan el riesgo:
- Diabetes, ERC, FEVI reducida.
- PCI compleja (≥3 stents, tronco, bifurcaciones).
- Historia de trombosis de stent o eventos recurrentes.
Se reconoce la evidencia reciente que avala DAPT abreviada (30–90 días) en pacientes seleccionados con alto riesgo hemorrágico.
3. Evaluación del riesgo hemorrágico
La evaluación del sangrado se basa en tres dimensiones:
- Procedimiento (factor más determinante).
- Consecuencias del sangrado (órganos críticos, espacios cerrados).
- Factores del paciente:
- Edad >65 años, ERC, hepatopatía.
- Anemia, trombocitopenia.
- Uso concomitante de AINE, doble terapia, INR lábil.
Clasificación de procedimientos:
- Riesgo mínimo (<0%)
Ej.: endoscopia sin biopsia, cirugía de catarata, procedimientos dentales simples. - Riesgo bajo–intermedio (0–2%)
Ej.: endoscopia con biopsia, colecistectomía, hernioplastía, cirugía mamaria. - Alto riesgo (≥2%)
Ej.: cirugía cardíaca, oncológica mayor, neurocirugía, anestesia neuroaxial.
Se enfatiza que la mayoría de sangrados ocurren en la primera semana, pero el riesgo persiste hasta 30 días.
4. Manejo perioperatorio de la anticoagulación
4.1. Antagonistas de vitamina K (warfarina/acenocumarol)
- Suspensión estándar:
- Warfarina: 5 días antes.
- Acenocumarol: 3 días antes.
- Objetivo preoperatorio: INR <1.2 (hasta <1.5 en algunos procedimientos).
- No se recomienda vitamina K preoperatoria electiva, por riesgo de resistencia posterior.
- Reinicio precoz (24 h), dado su inicio de acción lento.
Terapia puente
- Solo en alto riesgo tromboembólico.
- LMWH a dosis terapéuticas.
- Última dosis: 24 h antes (½ dosis).
- Evidencia sólida muestra ↑ sangrado sin ↓ trombosis en riesgo no alto.
4.2. Anticoagulantes orales directos (DOAC)
Principios clave:
- No usar terapia puente.
- Ajustar suspensión según:
- Tipo de DOAC.
- Función renal (CrCl Cockcroft-Gault).
- Riesgo hemorrágico del procedimiento.
Ejemplos:
- Apixabán/rivaroxabán:
- Riesgo bajo: suspender 24 h.
- Riesgo alto: 48 h.
- Dabigatrán:
- Mayor dependencia renal.
- Puede requerir 72–96 h si CrCl <50 mL/min.
Reinicio:
- 24 h si hemostasia adecuada.
- 48–72 h si alto riesgo hemorrágico.
5. Procedimientos de riesgo hemorrágico mínimo
En estos procedimientos:
- No se interrumpe sistemáticamente la anticoagulación.
- DOAC: omitir dosis del día del procedimiento.
- Reiniciar lo antes posible (idealmente al día siguiente).
Este enfoque reduce trombosis sin incrementar sangrado (evidencia grado B–A).
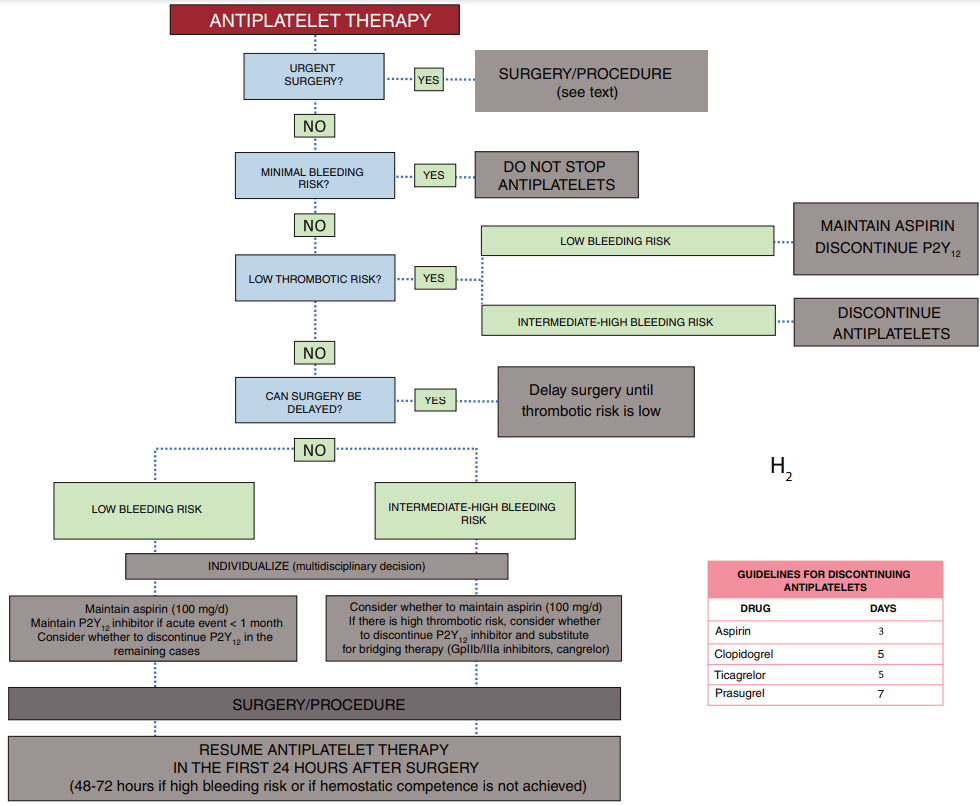
6. Manejo perioperatorio de la antiagregación
Antiagregación simple
- Aspirina ≤100 mg puede mantenerse en muchos procedimientos.
- Suspender si riesgo hemorrágico intermedio–alto y riesgo trombótico bajo.
Inhibidores P2Y12
- Clopidogrel / ticagrelor: suspender 5 días.
- Prasugrel: 7 días.
- Excepciones: cirugía coronaria (ticagrelor 3 días).
Doble antiagregación
- Si <30 días post-evento: priorizar continuar aspirina.
- Suspender P2Y12 si sangrado relevante.
- Bridging con cangrelor o GP IIb/IIIa: solo casos excepcionales, multidisciplinarios.
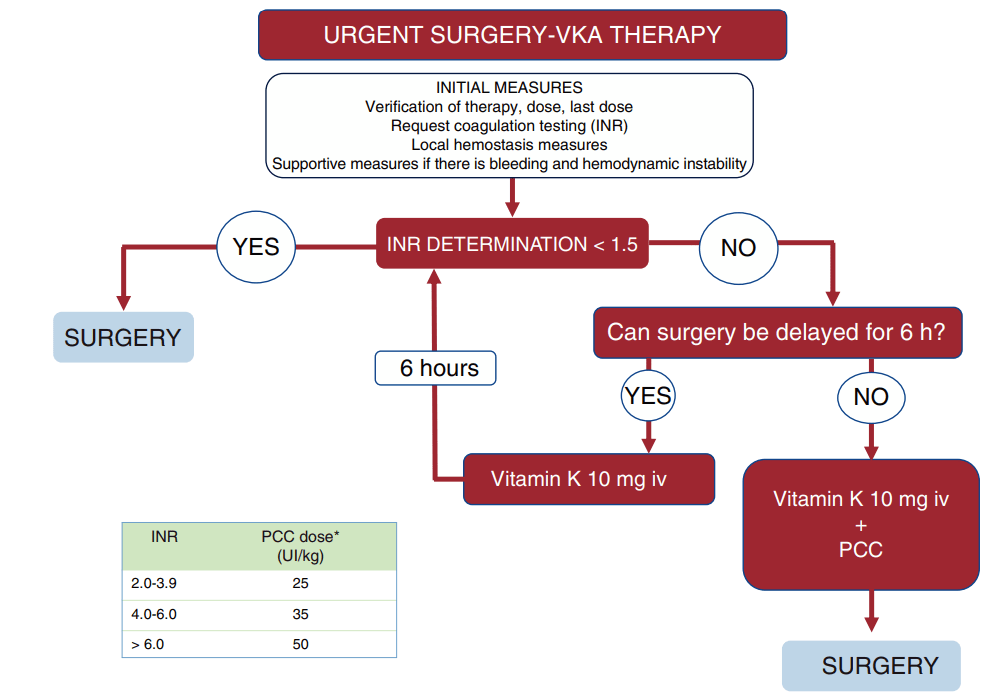
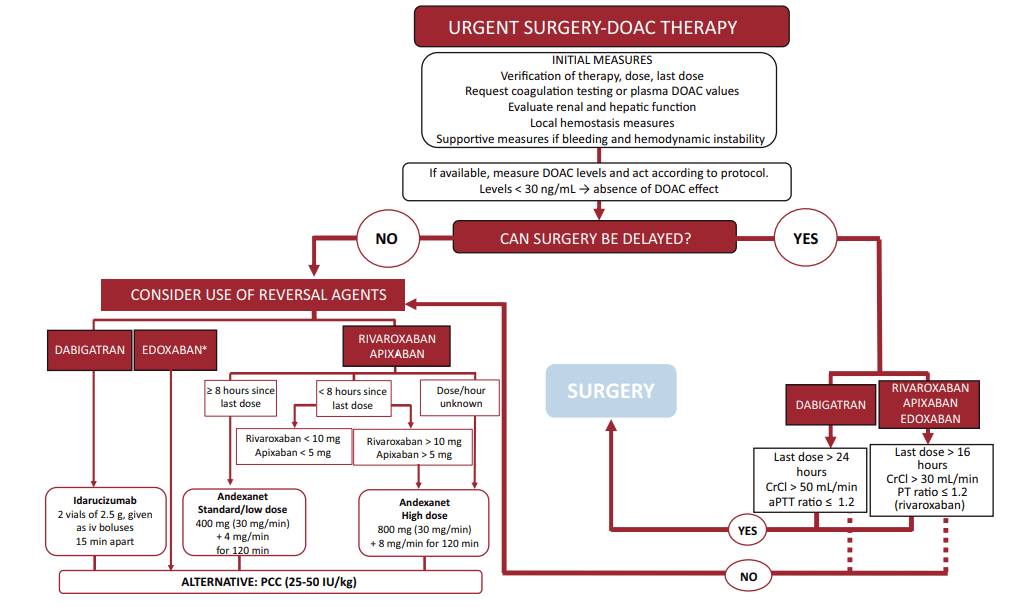
7. Cirugía urgente y emergente
Anticoagulación
- Emergente (<6 h): suspender fármaco + reversión si disponible.
- VKA:
- Vitamina K IV + PCC (preferido sobre plasma).
- DOAC:
- Idarucizumab (dabigatrán).
- Andexanet alfa (apixabán/rivaroxabán).
- PCC si reversor no disponible.
Antiagregación
- No debe retrasar cirugía urgente.
- Transfusión plaquetaria solo si sangrado activo.
- Ticagrelor: respuesta limitada a plaquetas.
8. Conclusiones y mensaje práctico
Este consenso propone un modelo equilibrado y pragmático, basado en:
- Evaluación individualizada del riesgo trombótico vs hemorrágico.
- Restricción del bridging a escenarios de verdadero alto riesgo.
- Reinicio precoz del tratamiento antitrombótico.
- Trabajo multidisciplinario como estándar.
👉 Mensaje central:
La interrupción innecesaria del tratamiento antitrombótico es tan peligrosa como su mantenimiento inapropiado.

Suscríbete para seguir leyendo
Suscríbete para obtener acceso al contenido íntegro de esta entrada y demás contenido exclusivo para suscriptores.

