El síndrome coronario agudo (ACS) se debe a la ruptura o erosión de una placa aterosclerótica inestable en las arterias coronarias, lo que genera trombosis parcial o completa y/o microémbolos, resultando en isquemia miocárdica. Se clasifica en tres condiciones clínicas:
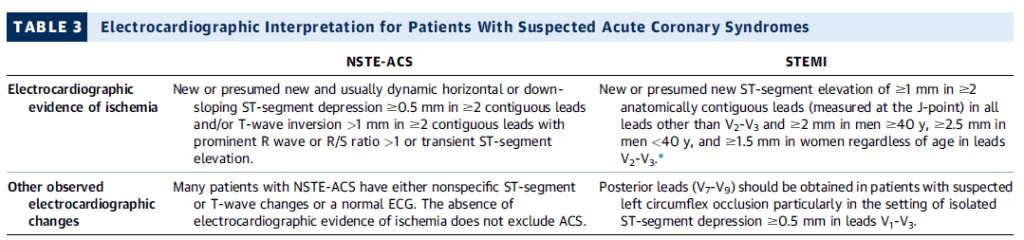
NSTE-ACS (SCA sin elevación del ST)
- Evidencia de isquemia:
- Depresión del segmento ST ≥0.5 mm en ≥2 derivaciones contiguas.
- Inversión de la onda T >1 mm en ≥2 derivaciones contiguas con onda R prominente o relación R/S >1.
- Elevación transitoria del segmento ST.
- Otros cambios:
- Puede haber cambios inespecíficos del ST o de la onda T, o un ECG normal.
- La ausencia de hallazgos en el ECG no excluye ACS.
STEMI (SCA con elevación del ST)
- Evidencia de isquemia:
- Elevación del ST ≥1 mm en ≥2 derivaciones contiguas (medida en el punto J).
- En V₂-V₃:
- ≥2 mm en hombres ≥40 años.
- ≥2.5 mm en hombres <40 años.
- ≥1.5 mm en mujeres (independientemente de la edad).
- Otros cambios:
- Se deben registrar derivaciones posteriores (V₇-V₉) en sospecha de oclusión de la circunfleja izquierda, especialmente si hay depresión del ST ≥0.5 mm en V₁-V₃.
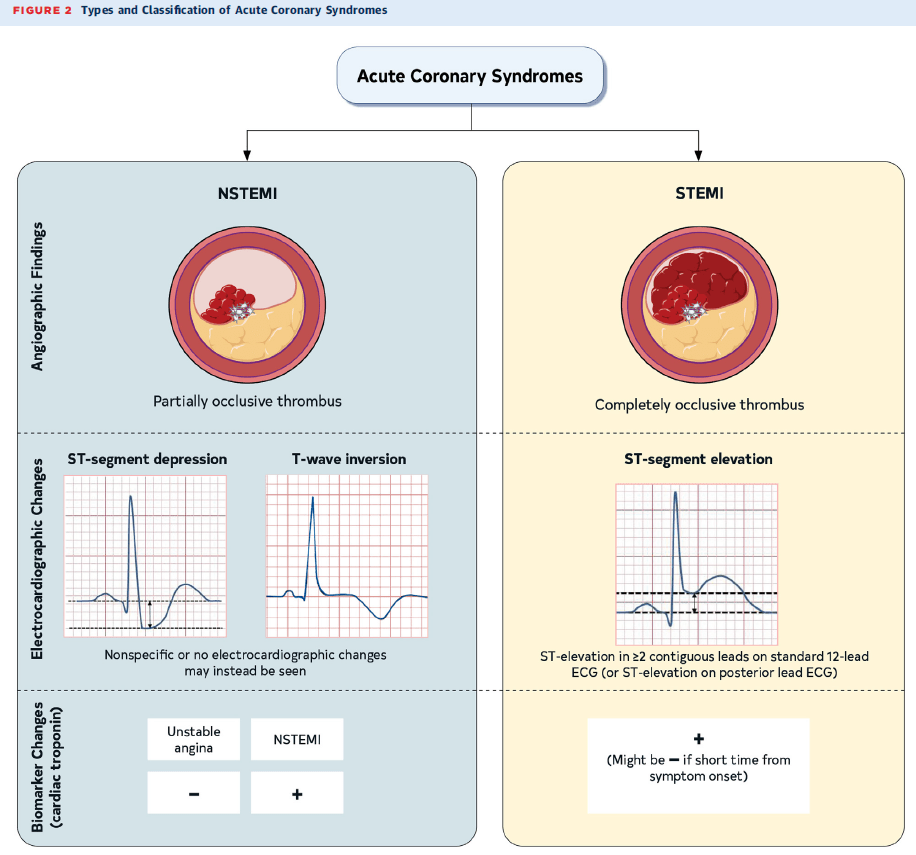
NSTEMI (Infarto sin elevación del ST)
- Hallazgos angiográficos: Trombo parcialmente oclusivo.
- Cambios electrocardiográficos:
- Depresión del ST.
- Inversión de la onda T (aunque el ECG puede ser inespecífico o normal).
- Biomarcadores: Troponinas positivas (+).
STEMI (Infarto con elevación del ST)
- Hallazgos angiográficos: Trombo completamente oclusivo.
- Cambios electrocardiográficos:
- Elevación del ST en ≥2 derivaciones contiguas en el ECG de 12 derivaciones o en derivaciones posteriores.
- Biomarcadores:
- Troponinas positivas (+), aunque pueden ser negativas en las primeras horas tras el inicio de síntomas.

Tipo 1
- Causa: Aterotrombosis coronaria aguda debido a ruptura o erosión de la placa aterosclerótica.
- Oclusión: Parcial o completa.
Tipo 2
- Causa: Desequilibrio entre el suministro y la demanda de oxígeno miocárdico.
- Sin aterotrombosis aguda.
Tipo 3
- Causa: Muerte cardíaca con síntomas de isquemia miocárdica y cambios electrocardiográficos isquémicos o arritmias ventriculares.
- Diagnóstico: No se logran tomar biomarcadores o se confirma post mortem en autopsia.
Tipo 4 (IAM post-PCI)
- 4a: Complicación del procedimiento, detectado ≤48 h tras una intervención coronaria percutánea (PCI).
- 4b: Trombo en un stent o su estructura.
- 4c: Reestenosis en un stent.
Tipo 5 (IAM post-CABG)
- Causa: Complicación del procedimiento, detectado ≤48 h después de una cirugía de bypass coronario (CABG).
Evaluación y manejo inicial del síndrome coronario agudo (ACS) sospechado
Recomendaciones para la evaluación prehospitalaria en ACS
1️⃣ ECG en los primeros 10 minutos
- Se debe realizar e interpretar un ECG de 12 derivaciones dentro de los 10 minutos del primer contacto médico (FMC) para identificar un STEMI (Clase 1, Evidencia B-NR).
2️⃣ ECG seriados en caso de ECG inicial no concluyente
- Si el primer ECG no muestra STEMI, se deben hacer ECGs seriados cuando la sospecha clínica es alta, los síntomas persisten o el paciente se deteriora (Clase 1, Evidencia C-LD).
Recomendaciones para STEMI en fase prehospitalaria
3️⃣ Traslado inmediato a hospital con PCI disponible
- Se recomienda el traslado inmediato en ambulancia a un hospital con capacidad de PCI primaria (PPCI), con un objetivo de tiempo FMC a dispositivo ≤90 minutos (Clase 1, Evidencia B-NR).
4️⃣ Notificación previa y activación del equipo de cateterismo
- El EMS debe notificar con anticipación al hospital receptor y activar el equipo de cateterismo para reducir el tiempo hasta la reperfusión (Clase 1, Evidencia B-NR).
Evaluación inicial en el hospital para pacientes con ACS confirmado o sospechado
Recomendaciones
1️⃣ ECG dentro de los primeros 10 minutos
- Se recomienda realizar e interpretar un ECG en los primeros 10 minutos para guiar el manejo (Clase 1, Evidencia B-NR).
2️⃣ ECG seriados si el primero no es diagnóstico
- Si el ECG inicial no muestra cambios claros, se deben realizar ECGs seriados, especialmente si la sospecha clínica es alta, los síntomas persisten o el paciente se deteriora (Clase 1, Evidencia B-NR).
3️⃣ Medición de troponinas (cTn)
- Se debe medir cTn lo antes posible, de preferencia usando troponina de alta sensibilidad (hs-cTn) (Clase 1, Evidencia B-NR).
4️⃣ Intervalo de medición de troponinas
- Si la cTn inicial es nondiagnóstica, se deben hacer mediciones repetidas:
- hs-cTn: cada 1 a 2 horas.
- cTn convencional: cada 3 a 6 horas (Clase 1, Evidencia B-NR).
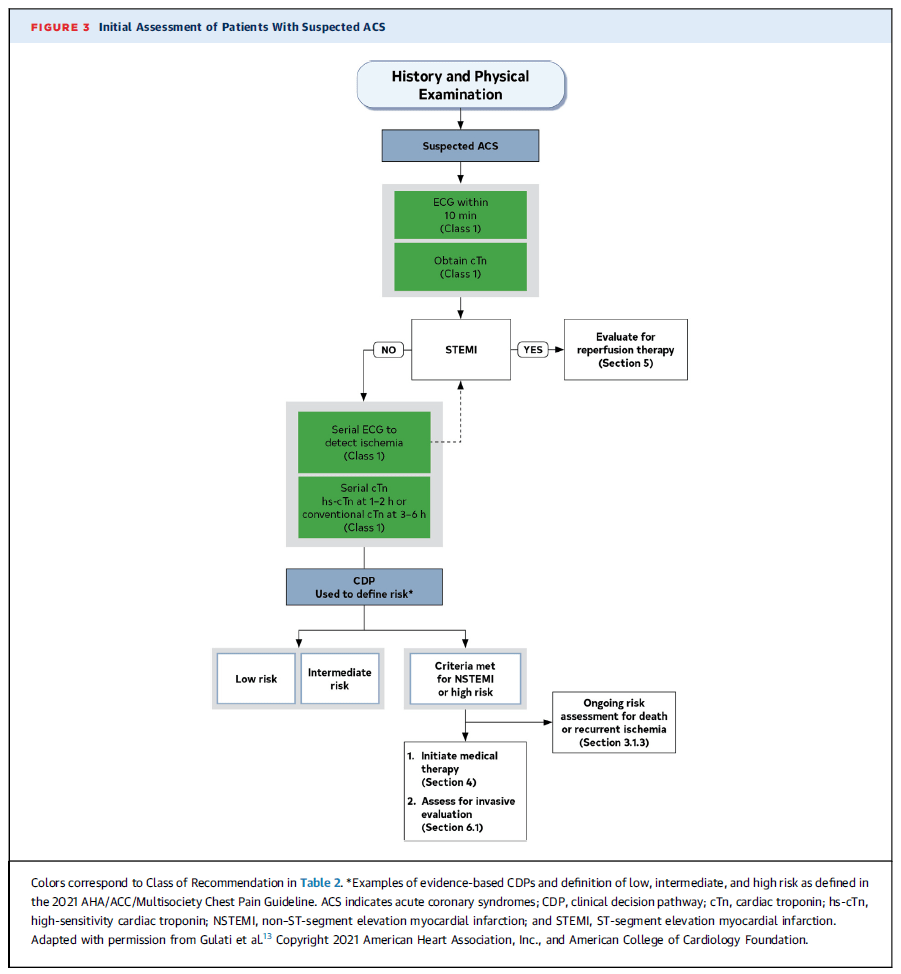
Evaluación inicial de pacientes con sospecha de ACS (Flujograma)
1️⃣ Historia clínica y examen físico
- Se inicia con la evaluación clínica de un paciente con sospecha de síndrome coronario agudo (ACS).
2️⃣ Pruebas iniciales
- ECG en los primeros 10 minutos (Clase 1).
- Medición de troponina (cTn) (Clase 1).
3️⃣ Evaluación del ECG
- Si hay STEMI → Evaluar para terapia de reperfusión (Sección 5).
- Si NO hay STEMI → Evaluar con pruebas adicionales:
- ECG seriados para isquemia (Clase 1).
- Troponinas seriadas:
- hs-cTn: cada 1-2 h.
- cTn convencional: cada 3-6 h (Clase 1).
4️⃣ Clasificación del riesgo con CDP (Clinical Decision Pathway)
- Bajo riesgo.
- Riesgo intermedio.
- NSTEMI o alto riesgo → Iniciar tratamiento médico (Sección 4) y evaluar para intervención invasiva (Sección 6.1).
5️⃣ Seguimiento
- Evaluación del riesgo continuo de muerte o isquemia recurrente (Sección 3.1.3).
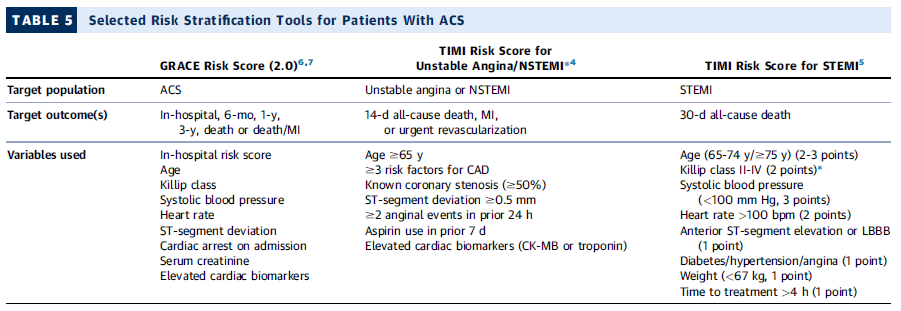
Herramientas de estratificación de riesgo en ACS
La tabla muestra tres escalas utilizadas para evaluar el riesgo en pacientes con síndrome coronario agudo (ACS).
1️⃣ GRACE Risk Score (2.0)
- Población objetivo: Todos los pacientes con ACS.
- Objetivos: Mortalidad hospitalaria, a 6 meses, 1 año y 3 años, o muerte/infarto.
- Variables:
- Edad.
- Killip class.
- Presión arterial sistólica.
- Frecuencia cardíaca.
- Declinación del ST.
- Paro cardíaco al ingreso.
- Creatinina sérica.
- Biomarcadores cardíacos elevados.
2️⃣ TIMI Risk Score para angina inestable/NSTEMI
- Población objetivo: Angina inestable o NSTEMI.
- Objetivos: Muerte por cualquier causa, IAM o revascularización urgente a 14 días.
- Variables:
- Edad ≥65 años.
- ≥3 factores de riesgo para CAD.
- Estenosis coronaria conocida ≥50%.
- Desviación del ST ≥0.5 mm.
- ≥2 episodios de angina en 24 h.
- Uso de aspirina en los últimos 7 días.
- Biomarcadores cardíacos elevados (CK-MB o troponina).
3️⃣ TIMI Risk Score para STEMI
- Población objetivo: Pacientes con STEMI.
- Objetivo: Mortalidad a 30 días.
- Variables:
- Edad (65-74 años = 2 puntos; ≥75 años = 3 puntos).
- Killip II-IV (2 puntos).
- Presión arterial sistólica <100 mmHg (3 puntos).
- Frecuencia cardíaca >100 lpm (2 puntos).
- Elevación del ST anterior o BRI (1 punto).
- Diabetes/hipertensión/angina (1 punto).
- Peso <67 kg (1 punto).
- Tiempo hasta tratamiento >4 h (1 punto).
Manejo de pacientes con paro cardíaco y sospecha de ACS
Recomendaciones
1️⃣ Traslado a un hospital con capacidad de PCI (Clase 1, Evidencia C-LD)
- Pacientes con paro cardíaco y STEMI que han sido reanimados deben ser trasladados a un centro con PCI disponible.
2️⃣ PPCI en pacientes con buen pronóstico (Clase 1, Evidencia B-NR)
- Pacientes reanimados que NO están en coma o que son comatosos con buen pronóstico y STEMI deben ser sometidos a PCI primaria para mejorar la supervivencia.
3️⃣ Evaluación individualizada en pacientes con mal pronóstico (Clase 2b, Evidencia C-LD)
- En pacientes comatosos, con mal pronóstico y STEMI, PPCI puede ser razonable, pero debe evaluarse caso por caso.
4️⃣ No se recomienda angiografía inmediata en pacientes sin STEMI (Clase 3, Evidencia A)
- Pacientes comatosos, estables eléctricamente y hemodinámicamente, sin evidencia de STEMI, NO deben recibir angiografía inmediata porque no ofrece beneficio.
Terapia de oxígeno en STEMI y NSTE-ACS
Recomendaciones
1️⃣ Oxígeno en pacientes con hipoxia (<90%) (Clase 1, Evidencia C-LD)
- En pacientes con ACS e hipoxia confirmada (saturación de oxígeno <90%), se recomienda oxígeno suplementario para elevar la saturación a ≥90%, mejorar el aporte de oxígeno al miocardio y reducir los síntomas anginosos.
2️⃣ No usar oxígeno rutinario si la saturación es ≥90% (Clase 3, Evidencia A)
- En pacientes con ACS y saturaciones de oxígeno ≥90%, el oxígeno suplementario rutinario NO está recomendado porque no mejora los desenlaces cardiovasculares.

| Medicamento | Vía | Dosis sugerida | Consideraciones |
|---|---|---|---|
| Nitroglicerina (SL) | Sublingual (tabletas, spray) | 0.3 – 0.4 mg cada 5 min, hasta un máximo de 3 dosis | Solo en pacientes hemodinámicamente estables con PA sistólica ≥90 mmHg. |
| Nitroglicerina (IV) | Intravenosa | Iniciar a 10 µg/min y titular según respuesta | Para angina persistente tras nitratos orales o si el ACS se asocia con hipertensión o edema pulmonar. Evitar en infarto de VD o PA sistólica <90 mmHg. Puede generar taquifilaxia tras 24 h. |
| Morfina (IV) | Intravenosa | 2-4 mg; repetir cada 5-15 min según necesidad (hasta 10 mg) | Para dolor resistente a otros fármacos antiisquémicos. Puede retrasar la acción de inhibidores P2Y12. Se debe monitorear efectos adversos. |
| Fentanilo (IV) | Intravenosa | 25-50 µg; repetir si es necesario (hasta 100 µg) | Para dolor resistente a otros fármacos antiisquémicos. Puede retrasar la acción de inhibidores P2Y12. Se debe monitorear efectos adversos. |
🔴 Precaución con nitratos
- No administrar si se ha usado un inhibidor de PDE5:
- Avanafil: en las últimas 12 h.
- Sildenafilo/Vardenafilo: en las últimas 24 h.
- Tadalafilo: en las últimas 48 h.
Terapia antiplaquetaria: Aspirina en ACS
Recomendación (Clase 1, Evidencia A)
- En pacientes con síndrome coronario agudo (ACS), se recomienda:
1️⃣ Dosis de carga oral inicial de aspirina.
2️⃣ Aspirina en dosis bajas diarias como mantenimiento.
🔹 Beneficio: Reduce la mortalidad y los eventos cardiovasculares adversos mayores (MACE).
Inhibidores orales P2Y12 durante la hospitalización en ACS
Para todos los pacientes con ACS (STEMI y NSTE-ACS)
1️⃣ Añadir un inhibidor P2Y12 a la aspirina para reducir eventos cardiovasculares adversos mayores (MACE) (Clase 1, Evidencia A).
2️⃣ Evitar prasugrel en pacientes con antecedente de EVC o AIT debido a peor desenlace clínico (Clase 3 – Daño, Evidencia B-R).
Manejo en hospitalización de pacientes con NSTE-ACS
3️⃣ En pacientes con PCI, prasugrel o ticagrelor son recomendados para reducir MACE y trombosis del stent (Clase 1, Evidencia B-R).
4️⃣ En pacientes sin estrategia invasiva, ticagrelor es recomendado para reducir MACE (Clase 1, Evidencia B-R).
5️⃣ Clopidogrel es una alternativa cuando prasugrel o ticagrelor no están disponibles, no son tolerados o están contraindicados (Clase 1, Evidencia B-R).
6️⃣ Si la angiografía será en >24 h, puede considerarse clopidogrel o ticagrelor (Clase 2b, Evidencia B-NR).
Manejo en hospitalización de pacientes con STEMI
7️⃣ En PCI primaria (PPCI), prasugrel o ticagrelor son recomendados para reducir MACE y trombosis del stent (Clase 1, Evidencia B-R).
8️⃣ Clopidogrel es una alternativa en PPCI cuando prasugrel o ticagrelor no están disponibles o son contraindicados (Clase 1, Evidencia C-LD).
9️⃣ En fibrinólisis, clopidogrel debe administrarse junto con el tratamiento para reducir mortalidad y MACE (Clase 1, Evidencia A).
Consideraciones de dosificación para terapia antiplaquetaria oral en ACS
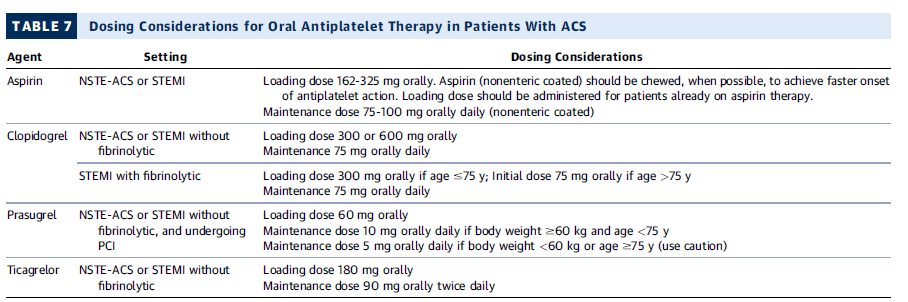
| Agente | Escenario | Dosis recomendada |
|---|---|---|
| Aspirina | NSTE-ACS o STEMI | Dosis de carga: 162-325 mg oral (masticar si es posible para efecto más rápido). Dosis de mantenimiento: 75-100 mg/día. |
| Clopidogrel | NSTE-ACS o STEMI sin fibrinolíticos | Dosis de carga: 300 o 600 mg oral. Dosis de mantenimiento: 75 mg/día. |
| STEMI con fibrinolíticos | Dosis de carga: 300 mg si ≤75 años; 75 mg si >75 años. Dosis de mantenimiento: 75 mg/día. | |
| Prasugrel | NSTE-ACS o STEMI sin fibrinolíticos y con PCI | Dosis de carga: 60 mg oral. Dosis de mantenimiento: 10 mg/día si peso ≥60 kg y edad <75 años. Reducir a 5 mg/día si peso <60 kg o edad ≥75 años (usar con precaución). |
| Ticagrelor | NSTE-ACS o STEMI sin fibrinolíticos | Dosis de carga: 180 mg oral. Dosis de mantenimiento: 90 mg dos veces al día. |
💡 Puntos clave:
- Aspirina: Masticar la dosis de carga para un efecto más rápido.
- Prasugrel: No usar en pacientes con EVC o AIT previos.
- Clopidogrel: Ajustar dosis en fibrinólisis según edad.
- Ticagrelor: Se administra dos veces al día, a diferencia de los otros agentes.
Elección inicial de inhibidor P2Y12 en pacientes con ACS sin necesidad de anticoagulante oral
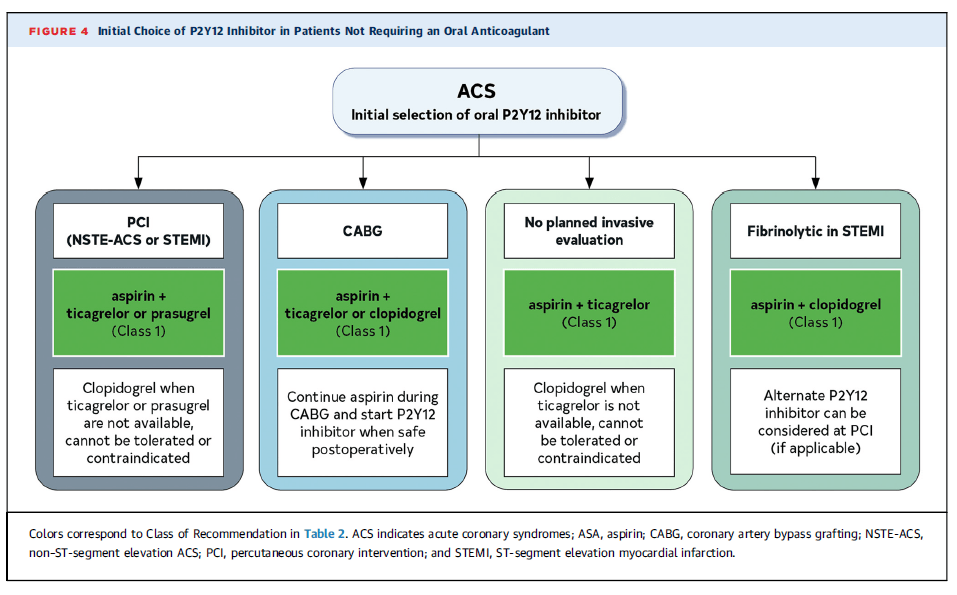
🔹 PCI (NSTE-ACS o STEMI)
✅ Aspirina + ticagrelor o prasugrel (Clase 1).
🔹 Clopidogrel es una opción si ticagrelor o prasugrel no están disponibles, no son tolerados o están contraindicados.
🔹 CABG (Bypass coronario)
✅ Aspirina + ticagrelor o clopidogrel (Clase 1).
🔹 Mantener aspirina durante la cirugía y reiniciar el inhibidor P2Y12 cuando sea seguro postoperatoriamente.
🔹 Sin evaluación invasiva planificada
✅ Aspirina + ticagrelor (Clase 1).
🔹 Clopidogrel es una opción si ticagrelor no está disponible, no es tolerado o está contraindicado.
🔹 Fibrinolisis en STEMI
✅ Aspirina + clopidogrel (Clase 1).
🔹 Se puede considerar otro inhibidor P2Y12 en caso de PCI posterior.
Manejo de inhibidores P2Y12 en pacientes que requieren CABG

| Fármaco | CABG electivo | CABG urgente |
|---|---|---|
| Clopidogrel | Suspender 5 días antes de la cirugía. | Suspender ≥24 h (idealmente) y realizar cirugía antes de 5 días si es razonable. |
| Prasugrel | Suspender 7 días antes de la cirugía. | Suspender ≥24 h (idealmente) y realizar cirugía antes de 7 días si es razonable. |
| Ticagrelor | Suspender 3-5 días antes de la cirugía. | Suspender ≥24 h (idealmente) y realizar cirugía antes de 5 días si es razonable. |
🔹 Reinicio post-CABG:
- Se recomienda reiniciar el inhibidor P2Y12 una vez que el riesgo de sangrado sea bajo, generalmente en 24-72 h.
Inhibición intravenosa de P2Y12 en ACS
🔹 Recomendación:
1️⃣ En pacientes con ACS que van a PCI y no han recibido un inhibidor P2Y12, el uso de cangrelor intravenoso puede ser razonable para reducir eventos isquémicos periprocedimiento (Clase 2b, Evidencia B-R).
💡 Puntos clave:
- Indicado en PCI cuando no se ha administrado previamente un inhibidor P2Y12 oral.
- Beneficio potencial: Disminución de eventos isquémicos en el procedimiento.
- Nivel de evidencia moderado (B-R), lo que sugiere beneficio pero con datos limitados.
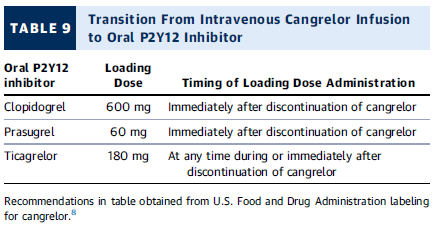
Transición de cangrelor IV a un inhibidor oral de P2Y12
| Inhibidor P2Y12 oral | Dosis de carga | Momento de administración |
|---|---|---|
| Clopidogrel | 600 mg | Inmediatamente después de suspender cangrelor. |
| Prasugrel | 60 mg | Inmediatamente después de suspender cangrelor. |
| Ticagrelor | 180 mg | En cualquier momento durante o inmediatamente después de suspender cangrelor. |
🔹 Puntos clave:
- Clopidogrel y prasugrel deben administrarse después de suspender cangrelor.
- Ticagrelor puede administrarse durante o inmediatamente después de la infusión de cangrelor.
Inhibidores de glicoproteína IIb/IIIa en ACS
🔹 Recomendaciones
1️⃣ Uso en PCI con alto trombo (Clase 2a, Evidencia C-LD)
- En pacientes con ACS sometidos a PCI con alta carga trombótica, no-reflow o flujo lento, el uso de un inhibidor IV o intracoronario de la GP IIb/IIIa puede ser razonable para mejorar el éxito del procedimiento y reducir el tamaño del infarto.
2️⃣ Evitar uso rutinario (Clase 3 – Daño, Evidencia B-R)
- No se recomienda su uso rutinario en ACS debido a la falta de beneficio isquémico y mayor riesgo de sangrado.
Anticoagulación parenteral en ACS
NSTE-ACS: Terapia anticoagulante temprana
1️⃣ Heparina no fraccionada (UFH) IV es útil para reducir eventos isquémicos (Clase 1, Evidencia B-R).
2️⃣ Si no se planea un enfoque invasivo temprano, enoxaparina o fondaparinux son alternativas recomendadas a la UFH (Clase 1, Evidencia B-R).
Anticoagulación en revascularización coronaria (CABG o PCI)
3️⃣ En pacientes con ACS que requieren revascularización en la misma hospitalización, la anticoagulación parenteral debe mantenerse hasta el procedimiento para reducir eventos isquémicos (Clase 1, Evidencia C-LD).
Anticoagulación en PCI en ACS (STEMI y NSTE-ACS)
4️⃣ UFH IV es útil para reducir eventos isquémicos en PCI (Clase 1, Evidencia C-EO).
5️⃣ Bivalirudina es una alternativa a UFH en STEMI para reducir mortalidad y sangrado (Clase 1, Evidencia B-R).
6️⃣ Bivalirudina puede ser razonable en NSTE-ACS como alternativa a UFH para reducir sangrado (Clase 2b, Evidencia B-R).
7️⃣ Enoxaparina IV puede considerarse en ACS como alternativa a UFH durante PCI para reducir eventos isquémicos (Clase 2b, Evidencia B-R).
8️⃣ Fondaparinux NO debe usarse en PCI debido al riesgo de trombosis del catéter (Clase 3 – Daño, Evidencia B-R).
Anticoagulación en STEMI con fibrinolíticos
9️⃣ Continuar anticoagulación parenteral hasta 8 días o hasta revascularización para reducir eventos isquémicos (Clase 1, Evidencia A).
🔟 Enoxaparina es el anticoagulante recomendado en pacientes sin estrategia invasiva (Clase 1, Evidencia A).
1️⃣1️⃣ Fondaparinux es una alternativa en STEMI sin estrategia invasiva (Clase 1, Evidencia B-R).
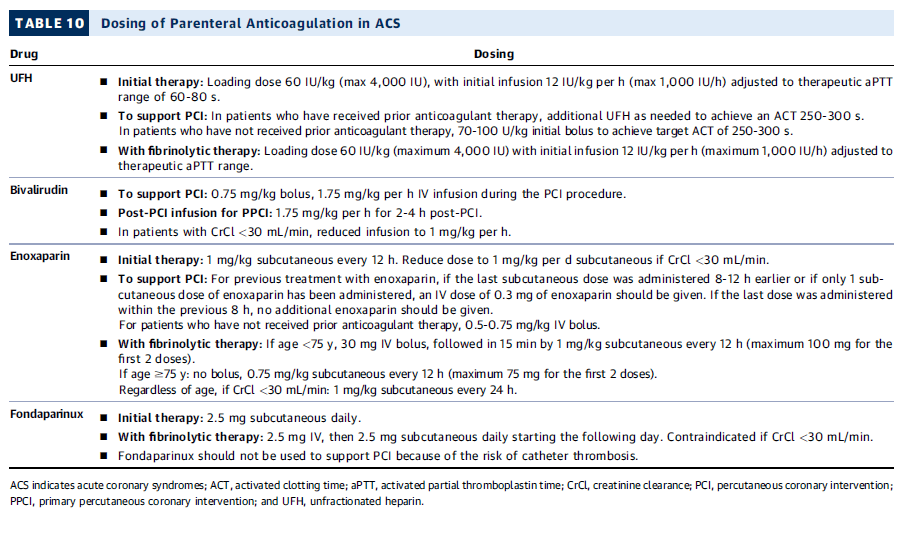
Dosificación de anticoagulantes parenterales en ACS
| Fármaco | Dosis recomendada |
|---|---|
| Heparina no fraccionada (UFH) | 🔹 Inicial: Bolo de 60 UI/kg (máx. 4,000 UI), seguido de infusión 12 UI/kg/h (máx. 1,000 UI/h), ajustado a aPTT 60-80 s. 🔹 En PCI: Ajustar según terapia previa, con bolo de 70-100 UI/kg si no recibió anticoagulación previa. 🔹 Con fibrinolíticos: Bolo de 60 UI/kg (máx. 4,000 UI), seguido de infusión 12 UI/kg/h, ajustado a aPTT terapéutico. |
| Bivalirudina | 🔹 En PCI: 0.75 mg/kg en bolo IV, seguido de 1.75 mg/kg/h durante el procedimiento. 🔹 Post-PCI: Infusión 1.75 mg/kg/h por 2-4 h post-PCI. 🔹 Si CrCl <30 mL/min: Reducir infusión a 1 mg/kg/h. |
| Enoxaparina | 🔹 Inicial: 1 mg/kg SC cada 12 h (reducir a 1 mg/kg SC cada 24 h si CrCl <30 mL/min). 🔹 En PCI: Si la última dosis SC fue hace 8-12 h, administrar bolo IV de 0.3 mg/kg. 🔹 Con fibrinolíticos: ➝ Si <75 años, bolo IV de 30 mg, seguido de 1 mg/kg SC cada 12 h (máx. 100 mg en las 2 primeras dosis). ➝ Si ≥75 años, no dar bolo IV y usar 0.75 mg/kg SC cada 12 h (máx. 75 mg en las 2 primeras dosis). |
| Fondaparinux | 🔹 Inicial: 2.5 mg SC/día (contraindicado si CrCl <30 mL/min). 🔹 Con fibrinolíticos: 2.5 mg SC/día desde el día siguiente. ❌ No usar en PCI por riesgo de trombosis del catéter. |
💡 Puntos clave:
- UFH es el estándar en PCI y fibrinolíticos.
- Bivalirudina puede usarse en PCI, especialmente en alto riesgo de sangrado.
- Enoxaparina es la mejor opción en fibrinolisis.
- Fondaparinux es seguro en fibrinolisis pero no debe usarse en PCI.
Manejo lipídico en ACS
1️⃣ Estatinas de alta intensidad recomendadas en ACS para reducir eventos cardiovasculares mayores (MACE) (Clase 1, Evidencia A).
2️⃣ Si LDL-C ≥70 mg/dL con estatina máxima tolerada, añadir otro agente hipolipemiante no estatínico para reducir MACE (Clase 1, Evidencia A).
3️⃣ Si intolerancia a estatinas, usar terapia hipolipemiante no estatínica para reducir LDL-C y MACE (Clase 1, Evidencia B-R).
4️⃣ Si LDL-C entre 55-69 mg/dL con estatina máxima tolerada, añadir otro hipolipemiante es razonable (Clase 2a, Evidencia B-R).
5️⃣ Considerar ezetimiba junto con estatina para reducir MACE (Clase 2b, Evidencia B-R).
💡 Puntos clave:
- Priorizar estatinas de alta intensidad.
- Agregar ezetimiba o inhibidores de PCSK9 si LDL-C sigue elevado.
- Opciones no estatínicas para pacientes intolerantes.
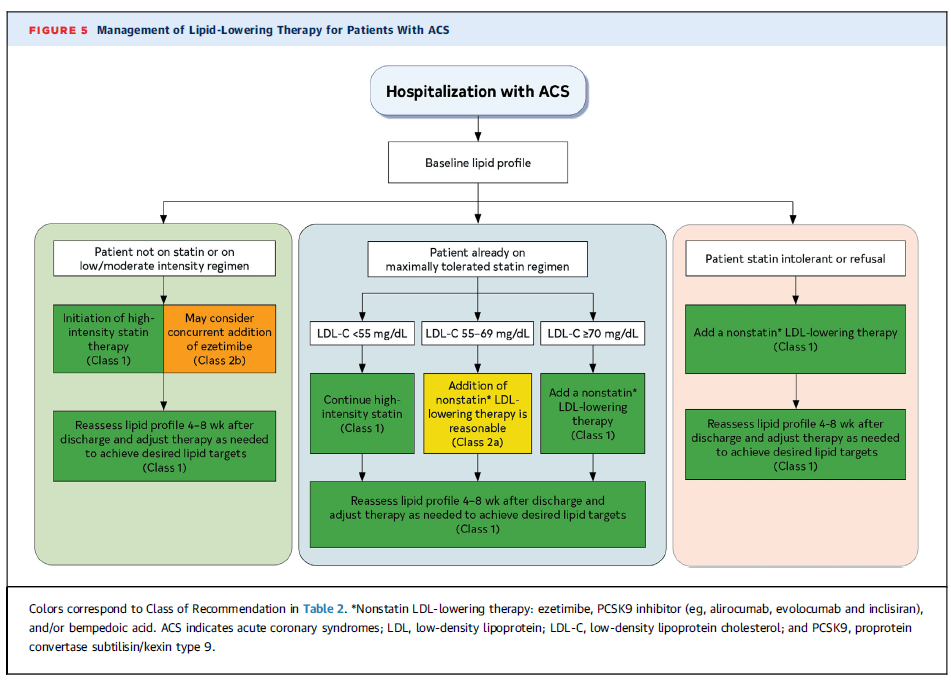
Manejo de la terapia hipolipemiante en ACS
🔹 Paciente sin estatinas o con régimen de baja/moderada intensidad
✅ Iniciar estatinas de alta intensidad (Clase 1).
🔸 Considerar agregar ezetimiba (Clase 2b).
📌 Reevaluar perfil lipídico en 4-8 semanas y ajustar según objetivos (Clase 1).
🔹 Paciente en estatina máxima tolerada
✅ Si LDL-C ≥70 mg/dL, agregar terapia no estatínica (Clase 1).
✅ Si LDL-C 55-69 mg/dL, considerar agregar terapia no estatínica (Clase 2a).
📌 Reevaluar perfil lipídico en 4-8 semanas y ajustar según objetivos (Clase 1).
🔹 Paciente intolerante a estatinas o que rechaza su uso
✅ Iniciar terapia no estatínica (Clase 1).
📌 Reevaluar perfil lipídico en 4-8 semanas y ajustar según objetivos (Clase 1).
💡 Opciones de terapia no estatínica:
- Ezetimiba.
- Inhibidores de PCSK9 (alirocumab, evolocumab, inclisiran).
- Ácido bempedoico.
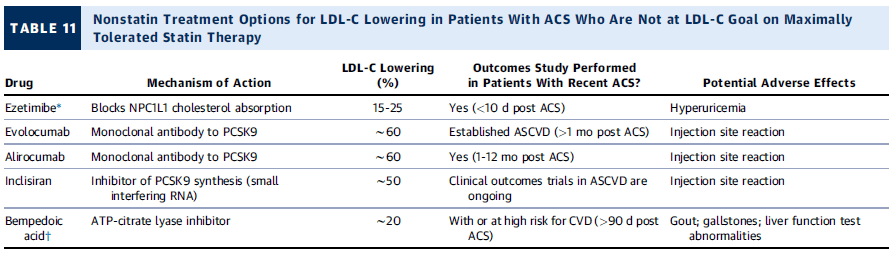
Opciones de tratamiento no estatínico para reducción de LDL-C en ACS
| Fármaco | Mecanismo de acción | Reducción de LDL-C (%) | Estudiado en ACS reciente | Efectos adversos |
|---|---|---|---|---|
| Ezetimiba | Bloquea la absorción de colesterol (NPC1L1) | 15-25% | Sí (<10 días post-ACS) | Hiperuricemia |
| Evolocumab | Anticuerpo monoclonal contra PCSK9 | ~60% | Sí (>1 mes post-ACS) | Reacciones en sitio de inyección |
| Alirocumab | Anticuerpo monoclonal contra PCSK9 | ~60% | Sí (9-12 meses post-ACS) | Reacciones en sitio de inyección |
| Inclisiran | Inhibidor de la síntesis de PCSK9 (RNA de interferencia) | ~50% | Ensayos clínicos en curso en ASCVD | Reacciones en sitio de inyección |
| Ácido bempedoico | Inhibidor de ATP-citrato liasa | ~20% | Sí, en alto riesgo de enfermedad CV (>90 días post-ACS) | Gota, cálculos biliares, alteraciones en pruebas hepáticas |
💡 Puntos clave:
- Ezetimiba es la opción más estudiada en el periodo agudo de ACS.
- Inhibidores de PCSK9 (evolocumab, alirocumab, inclisiran) tienen mayor reducción de LDL-C (~50-60%).
- Ácido bempedoico es una alternativa para pacientes con alto riesgo cardiovascular y ACS >90 días.
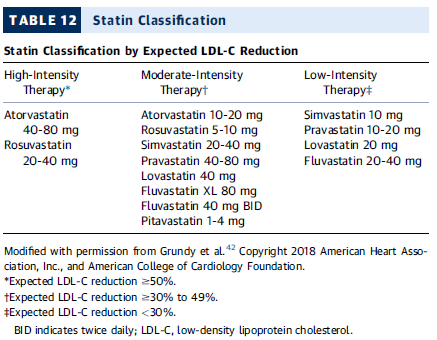
Clasificación de estatinas según reducción esperada de LDL-C
| Terapia | Fármacos y dosis | Reducción esperada de LDL-C |
|---|---|---|
| Alta intensidad | ✅ Atorvastatina 40-80 mg ✅ Rosuvastatina 20-40 mg | ≥50% |
| Moderada intensidad | ✅ Atorvastatina 10-20 mg ✅ Rosuvastatina 5-10 mg ✅ Simvastatina 20-40 mg ✅ Pravastatina 40-80 mg ✅ Lovastatina 40 mg ✅ Fluvastatina XL 80 mg ✅ Fluvastatina 40 mg BID ✅ Pitavastatina 1-4 mg | 30-49% |
| Baja intensidad | ✅ Simvastatina 10 mg ✅ Pravastatina 10-20 mg ✅ Lovastatina 20 mg ✅ Fluvastatina 20-40 mg | <30% |
💡 Puntos clave:
- Alta intensidad (atorvastatina 40-80 mg, rosuvastatina 20-40 mg) es la recomendada en ACS.
- Si no se tolera alta intensidad, usar estatinas de moderada intensidad.
- Baja intensidad solo en casos con intolerancia grave.
Terapia con Betabloqueadores en ACS
✅ Recomendación:
1️⃣ En pacientes con ACS sin contraindicaciones, iniciar betabloqueadores orales dentro de las primeras 24 horas para reducir el riesgo de reinfarto y arritmias ventriculares (Clase 1, Evidencia A).
💡 Puntos clave:
- Beneficio comprobado en reducir mortalidad y complicaciones.
- Contraindicaciones: Insuficiencia cardíaca descompensada, shock cardiogénico, bradicardia severa, bloqueo AV avanzado.
Inhibidores del Sistema Renina-Angiotensina-Aldosterona en ACS
✅ Recomendaciones:
1️⃣ Pacientes de alto riesgo (Clase 1, Evidencia A)
- Indicado en LVEF ≤40%, hipertensión, diabetes o STEMI anterior.
- Usar un IECA o ARA-II para reducir mortalidad y MACE.
2️⃣ Pacientes con ACS, LVEF ≤40%, síntomas de IC o diabetes (Clase 1, Evidencia B-R)
- Indicado un antagonista de receptor de mineralocorticoides (ej. espironolactona) para reducir mortalidad y MACE.
3️⃣ Pacientes sin alto riesgo (Clase 2a, Evidencia A)
- Un IECA o ARA-II puede ser razonable para reducir MACE.
💡 Puntos clave:
Espironolactona o eplerenona en disfunción ventricular con IC/diabetes
IECA de primera línea en pacientes de alto riesgo.
ARA-II como alternativa si IECA no es tolerado.
Manejo del STEMI: Estrategias de Reperfusión
Sistemas regionales de atención para STEMI
✅ Recomendación (Clase 1, Evidencia B-NR):
1️⃣ Todas las comunidades deben crear y mantener sistemas regionales de atención para STEMI, que coordinen el manejo prehospitalario y hospitalario, con el objetivo de:
- Reducir el tiempo isquémico total.
- Mejorar la supervivencia en pacientes con STEMI.
💡 Puntos clave:
- Integración de EMS (servicios de emergencia), hospitales y centros de PCI.
- Activación temprana del equipo de reperfusión.
- Enfoque en disminuir el tiempo hasta la reperfusión.
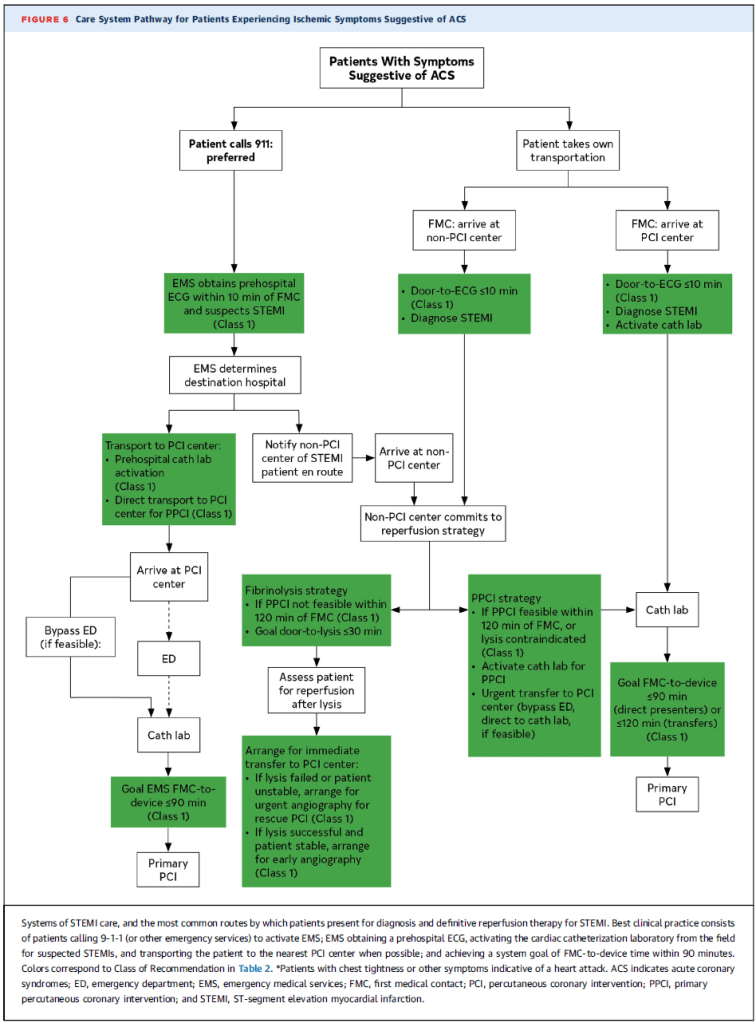
Intervención coronaria percutánea primaria (PPCI) en STEMI
✅ Recomendaciones principales:
1️⃣ STEMI <12 h desde el inicio de síntomas:
- Realizar PPCI con objetivo FMC-to-device ≤90 min o ≤120 min si requiere traslado (Clase 1, Evidencia A).
2️⃣ ACS con shock cardiogénico o inestabilidad hemodinámica:
- Revascularización de emergencia (PCI o CABG) independientemente del tiempo desde el inicio de síntomas (Clase 1, Evidencia B-R).
3️⃣ STEMI entre 12-24 h desde el inicio de síntomas:
- PPCI razonable para mejorar desenlaces clínicos (Clase 2a, Evidencia B-NR).
4️⃣ STEMI >24 h con isquemia activa o arritmias graves:
- PPCI razonable si hay evidencia de isquemia en curso o arritmia letal (Clase 2a, Evidencia C-LD).
🚫 Cuándo NO hacer PPCI:
5️⃣ STEMI >24 h sin isquemia en curso, sin IC grave ni arritmias peligrosas:
- No realizar PPCI, ya que no aporta beneficio (Clase 3 – Sin beneficio, Evidencia B-R).
💡 Puntos clave:
- Prioridad en PPCI dentro de las primeras 12 h.
- No hay límite de tiempo si el paciente está inestable.
- Después de 24 h, PPCI solo si hay isquemia activa o arritmias graves
Cirugía de revascularización coronaria urgente (CABG) en STEMI
✅ Recomendación (Clase 2a, Evidencia B-NR):
1️⃣ En pacientes con STEMI en quienes la PCI no es factible o no fue exitosa, y con una gran área de miocardio en riesgo, la cirugía de revascularización urgente (CABG) puede ser efectiva para mejorar los desenlaces clínicos.
💡 Puntos clave:
- Considerar CABG de urgencia si:
- PCI fallida.
- Obstrucción coronaria extensa.
- Gran cantidad de miocardio en riesgo.
Reperfusión en hospitales sin capacidad de PCI
✅ Recomendaciones principales:
1️⃣ STEMI con tiempo estimado FMC-to-device ≤120 min o contraindicación a fibrinolíticos:
- Trasladar a un hospital con PCI para PPCI (Clase 1, Evidencia A).
2️⃣ STEMI <12 h con retraso >120 min para PPCI:
- Administrar fibrinólisis en pacientes sin contraindicación para reducir MACE (Clase 1, Evidencia A).
3️⃣ STEMI entre 12-24 h:
- Transferencia a un hospital con PCI es razonable para reducir el tamaño del infarto y MACE (Clase 2a, Evidencia B-NR).
🚫 Cuándo NO administrar fibrinolíticos:
4️⃣ Depresión del ST sin sospecha de STEMI posterior verdadero:
- No dar fibrinólisis por alto riesgo de EVC hemorrágico y sangrado mayor (Clase 3 – Daño, Evidencia B-R).
💡 Puntos clave:
- PCI es preferida, pero si hay retraso >120 min, usar fibrinolíticos.
- Evitar fibrinolíticos en depresión del ST, excepto en STEMI posterior.

Agentes fibrinolíticos específicos para STEMI
| Fármaco | Dosis |
|---|---|
| Tenecteplase (TNK-tPA) | Bolo IV único ajustado por peso. |
| Reteplase (rPA) | Dos bolos IV de 10 U, administrados con 30 min de diferencia (cada bolo en 2 min). |
| Alteplase (tPA) | Infusión IV ajustada por peso durante 90 min. |
💡 Puntos clave:
- Tenecteplase: Más fácil de administrar (bolo único).
- Reteplase: Se administra en dos bolos separados.
- Alteplase: Infusión más prolongada (90 min).
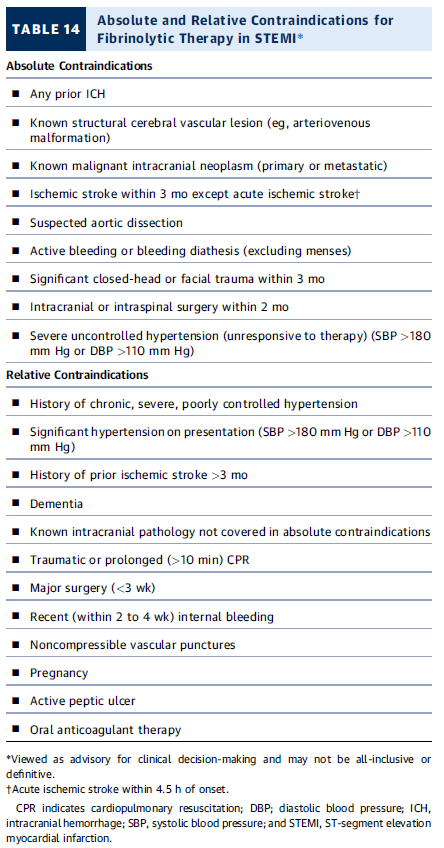
Contraindicaciones para terapia fibrinolítica en STEMI
✅ Contraindicaciones absolutas (NO administrar fibrinolíticos):
- Hemorragia intracraneal (ICH) previa.
- Lesión estructural cerebral (ej. malformación arteriovenosa).
- Neoplasia intracraneal maligna.
- ACV isquémico en los últimos 3 meses (excepto ACV agudo <4.5 h).
- Disección aórtica sospechada.
- Sangrado activo o diátesis hemorrágica (excepto menstruación).
- Trauma craneoencefálico cerrado severo o facial en los últimos 3 meses.
- Cirugía intracraneal o intraespinal en los últimos 2 meses.
- Hipertensión severa no controlada (PAS >180 mmHg o PAD >110 mmHg).
⚠ Contraindicaciones relativas (evaluar riesgo-beneficio):
- Hipertensión crónica severa mal controlada.
- Hipertensión en presentación (PAS >180 mmHg o PAD >110 mmHg).
- ACV isquémico previo (>3 meses).
- Demencia.
- Patología intracraneal no incluida en las absolutas.
- RCP traumática o prolongada (>10 min).
- Cirugía mayor reciente (<3 semanas).
- Sangrado interno reciente (últimas 2-4 semanas).
- Punciones vasculares no compresibles.
- Embarazo.
- Úlcera péptica activa.
- Uso de anticoagulantes orales.
💡 Puntos clave:
- Absolutas → Fibrinolisis está contraindicada.
- Relativas → Evaluar riesgo/beneficio antes de administrar.
Angiografía coronaria y PCI después de fibrinolíticos en STEMI
✅ Recomendaciones:
1️⃣ Traslado inmediato a un centro con PCI después de fibrinolisis (Clase 1, Evidencia A).
2️⃣ Si se sospecha reperfusión fallida, realizar angiografía inmediata y PCI de rescate para reducir muerte o infarto recurrente (Clase 1, Evidencia B-R).
3️⃣ Si la fibrinolisis fue exitosa, realizar angiografía temprana entre 2-24 h para evaluar necesidad de PCI y reducir mortalidad (Clase 1, Evidencia B-R).
💡 Puntos clave:
- Fibrinólisis no excluye PCI: Todos los pacientes deben ser evaluados para revascularización.
- PCI de rescate inmediata si signos de reperfusión fallida.
- Angiografía en 2-24 h en casos estables para planificación de revascularización.
Enfoque invasivo rutinario o selectivo en NSTE-ACS
✅ Recomendaciones:
1️⃣ Pacientes con NSTE-ACS de riesgo intermedio-alto:
- Enfoque invasivo recomendado para revascularización durante la hospitalización para reducir MACE (Clase 1, Evidencia A).
2️⃣ Pacientes con NSTE-ACS de bajo riesgo:
- Estrategia invasiva o selectiva razonable para identificar quiénes necesitan revascularización (Clase 1, Evidencia A).
🔹 Momento de la angiografía en estrategia invasiva:
3️⃣ NSTE-ACS con angina refractaria, inestabilidad hemodinámica o eléctrica:
- Estrategia invasiva inmediata con revascularización (Clase 1, Evidencia C-LD).
4️⃣ NSTE-ACS de alto riesgo:
- Estrategia invasiva temprana (<24 h) es razonable para reducir MACE (Clase 2a, Evidencia B-R).
5️⃣ NSTE-ACS sin alto riesgo pero con estrategia invasiva planificada:
- Angiografía antes del alta es razonable para reducir MACE (Clase 2a, Evidencia B-R).
💡 Puntos clave:
- Estrategia invasiva prioritaria en pacientes de riesgo alto o inestabilidad.
- Evaluación caso por caso en pacientes de bajo riesgo.
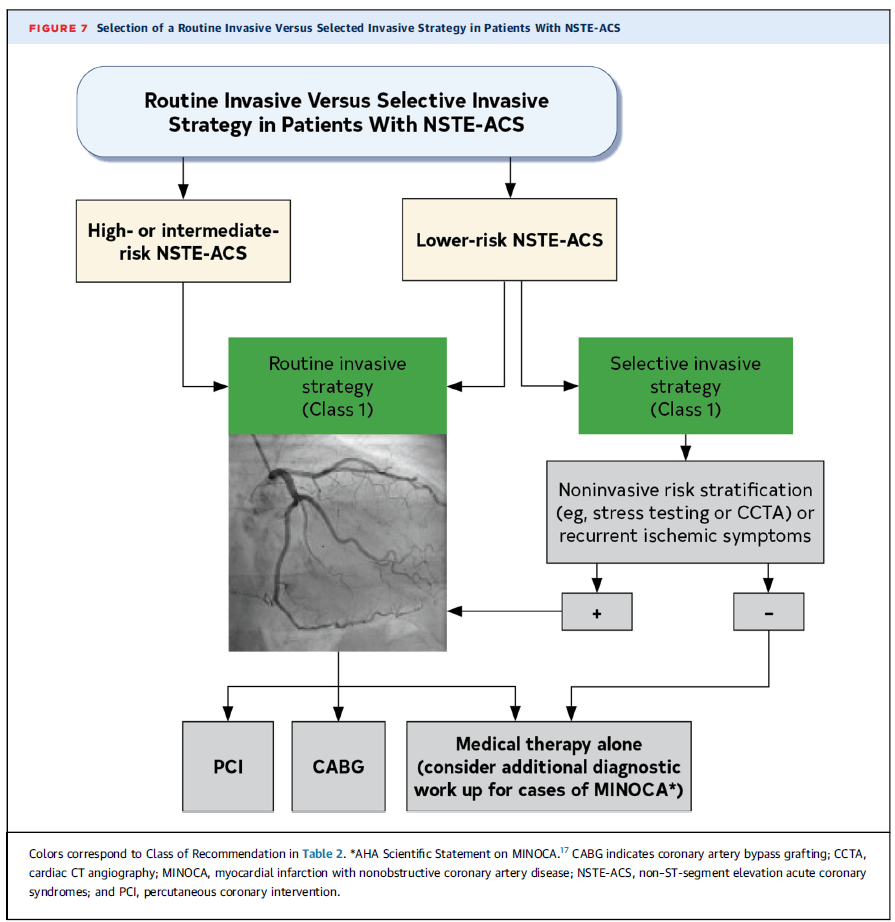
Estrategia invasiva rutinaria vs. selectiva en NSTE-ACS
🔹 Pacientes con NSTE-ACS de riesgo intermedio-alto
✅ Estrategia invasiva rutinaria (Clase 1).
🔸 Se procede a PCI o CABG según hallazgos angiográficos.
🔹 Pacientes con NSTE-ACS de bajo riesgo
✅ Estrategia invasiva selectiva (Clase 1).
🔸 Se realiza estratificación de riesgo no invasiva (prueba de esfuerzo, angio-TC).
- Si es positiva → PCI o CABG según hallazgos.
- Si es negativa → Manejo médico (considerar evaluación adicional en MINOCA*).
💡 Puntos clave:
- PCI o CABG si hay enfermedad significativa.
- Estrategia selectiva en bajo riesgo con pruebas adicionales.
- Considerar MINOCA (infarto sin enfermedad obstructiva).
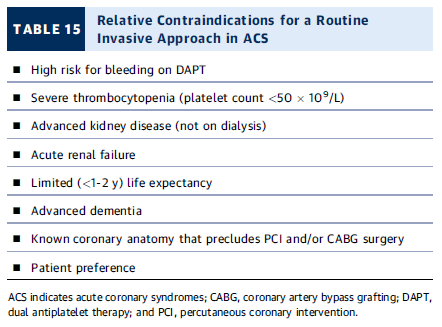
Contraindicaciones relativas para un enfoque invasivo en ACS
🚫 Situaciones en las que el enfoque invasivo puede no ser adecuado:
- Alto riesgo de sangrado con terapia antiplaquetaria dual (DAPT).
- Trombocitopenia severa (plaquetas <50 × 10⁹/L).
- Enfermedad renal avanzada (no en diálisis).
- Insuficiencia renal aguda.
- Esperanza de vida limitada (<1-2 años).
- Demencia avanzada.
- Anatomía coronaria que impide PCI o CABG.
- Preferencia del paciente.
💡 Puntos clave:
- Evaluación individualizada del riesgo/beneficio en estos casos.
- En pacientes frágiles o con alto riesgo de sangrado, considerar manejo médico optimizado.
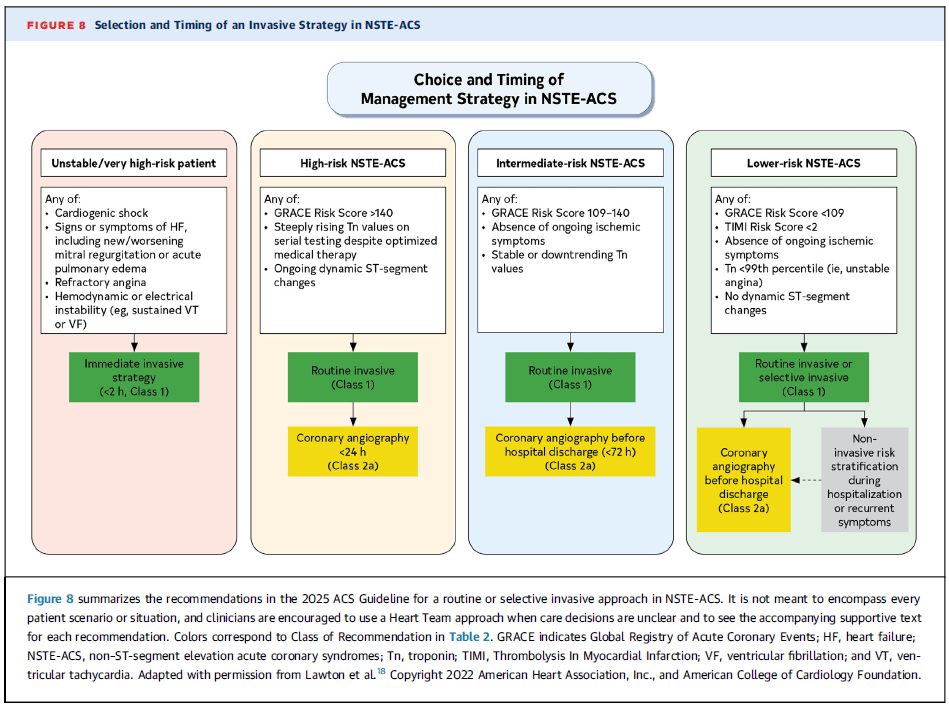
Selección y momento de la estrategia invasiva en NSTE-ACS
🔴 Paciente inestable / muy alto riesgo
✅ Estrategia invasiva inmediata (<2 h, Clase 1) si presenta:
- Shock cardiogénico.
- Insuficiencia cardíaca aguda (nuevo/peor edema pulmonar o insuficiencia mitral).
- Angina refractaria.
- Inestabilidad hemodinámica o eléctrica (TV/FV sostenida).
🟠 NSTE-ACS de alto riesgo
✅ Estrategia invasiva rutinaria (Clase 1) si presenta:
- GRACE >140.
- Troponina en ascenso pronunciado a pesar de tratamiento médico.
- Cambios dinámicos del ST.
📌 Coronariografía en <24 h (Clase 2a).
🟡 NSTE-ACS de riesgo intermedio
✅ Estrategia invasiva rutinaria (Clase 1) si presenta:
- GRACE 109-140.
- Troponina estable o en descenso.
📌 Coronariografía antes del alta (<72 h, Clase 2a).
🟢 NSTE-ACS de bajo riesgo
✅ Estrategia invasiva o selectiva (Clase 1) si presenta:
- GRACE <109 o TIMI <2.
- Sin síntomas isquémicos activos.
- Troponina <99p (angina inestable).
- Sin cambios dinámicos del ST.
📌 Coronariografía antes del alta (Clase 2a) o evaluación no invasiva.
💡 Puntos clave:
- Inestabilidad → angiografía inmediata (<2 h).
- Alto riesgo → angiografía en <24 h.
- Intermedio → angiografía en <72 h.
- Bajo riesgo → evaluación no invasiva o angiografía antes del alta.
Acceso vascular para PCI en ACS
✅ Recomendación (Clase 1, Evidencia A):
1️⃣ En pacientes con ACS sometidos a PCI, se prefiere el acceso radial sobre el femoral para reducir sangrado, complicaciones vasculares y mortalidad.
💡 Puntos clave:
- Menor riesgo de sangrado y complicaciones vasculares con acceso radial.
- Acceso femoral reservado si el radial no es viable o si se requiere otro abordaje.
Uso de trombectomía por aspiración en STEMI
🚫 Recomendación (Clase 3 – Sin beneficio, Evidencia A):
1️⃣ En pacientes con STEMI sometidos a PPCI, la trombectomía manual por aspiración no debe realizarse de manera rutinaria, ya que no aporta beneficio clínico.
💡 Puntos clave:
- No mejora desenlaces clínicos y puede aumentar el riesgo de eventos adversos.
- PCI con stent sigue siendo el tratamiento estándar.
- Puede considerarse en casos seleccionados con carga trombótica masiva.
Uso de imagen intracoronaria en ACS
✅ Recomendación (Clase 1, Evidencia A):
1️⃣ En pacientes con ACS que requieren implantación de stent en el tronco coronario izquierdo o en lesiones complejas, se recomienda el uso de ultrasonido intravascular (IVUS) o tomografía de coherencia óptica (OCT) para guiar el procedimiento y reducir eventos isquémicos.
💡 Puntos clave:
- IVUS y OCT mejoran la precisión en la colocación del stent.
- Útil en lesiones complejas y tronco coronario izquierdo.
- Asociado con menor tasa de reestenosis y trombosis del stent.
Manejo de enfermedad multivaso en STEMI
✅ Recomendaciones:
1️⃣ Paciente estable con enfermedad multivaso (MVD):
- Tras PCI exitosa del vaso culpable, realizar PCI de arterias no culpables con estenosis significativa para reducir muerte e infarto y mejorar calidad de vida (Clase 1, Evidencia A).
2️⃣ Paciente con MVD compleja:
- Cirugía de revascularización (CABG) puede ser una opción razonable, especialmente si hay afectación de la DA proximal o tronco coronario izquierdo (Clase 2a, Evidencia C-EO).
3️⃣ Paciente estable con MVD de baja complejidad (no candidato a CABG):
- PCI multivaso en la misma intervención puede ser preferible sobre una estrategia escalonada para reducir eventos cardiovasculares (Clase 2b, Evidencia B-R).
🚫 Cuándo NO hacer PCI multivaso:
4️⃣ Paciente con shock cardiogénico:
- No realizar PCI de arterias no culpables en la fase aguda, ya que aumenta el riesgo de muerte o insuficiencia renal (Clase 3 – Daño, Evidencia B-R).
💡 Puntos clave:
- PCI diferida del multivaso es preferida en pacientes estables.
- CABG es opción en enfermedad compleja.
- Evitar PCI multivaso en shock cardiogénico agudo.
Manejo de enfermedad multivaso en NSTE-ACS
✅ Recomendaciones:
1️⃣ Elección entre CABG o PCI en NSTE-ACS con MVD:
- Basado en la complejidad de la enfermedad y comorbilidades (Clase 1, Evidencia C-EO).
🔹 Candidatos a PCI:
2️⃣ Paciente estable con NSTE-ACS y MVD (sin tronco izquierdo):
- PCI de lesiones no culpables puede realizarse en la misma intervención o de manera escalonada para reducir MACE (Clase 1, Evidencia B-R).
3️⃣ Si se considera PCI multivaso:
- Evaluación fisiológica de la estenosis (ej. FFR/iFR) es razonable para guiar la revascularización (Clase 2b, Evidencia B-R).
🚫 Cuándo NO hacer PCI multivaso:
4️⃣ Paciente con NSTE-ACS en shock cardiogénico:
- No realizar PCI de arterias no culpables en la fase aguda, ya que aumenta el riesgo de muerte o insuficiencia renal (Clase 3 – Daño, Evidencia B-R).
💡 Puntos clave:
- Evaluar PCI vs CABG según la complejidad anatómica y clínica.
- PCI diferida o guiada por fisiología es preferida en pacientes estables.
- Evitar PCI multivaso en shock cardiogénico agudo.

Elección entre CABG o PCI en NSTE-ACS con enfermedad multivaso (MVD)
✅ CABG es preferido sobre PCI en:
- Estenosis significativa del tronco coronario izquierdo con enfermedad coronaria compleja.
- MVD extensa, compleja o difusa.
- Diabetes mellitus con afectación de la DA.
- MVD o tronco coronario con disfunción ventricular severa.
💡 Puntos clave:
- CABG mejora supervivencia en anatomía compleja o disfunción ventricular.
- PCI es opción en MVD menos compleja o cuando CABG no es viable.
Manejo del shock cardiogénico en ACS
✅ Revascularización en shock cardiogénico:
1️⃣ En pacientes con ACS y shock cardiogénico o inestabilidad hemodinámica:
- Revascularización urgente del vaso culpable mediante PCI o CABG mejora la supervivencia, sin importar el tiempo desde el inicio de los síntomas (Clase 1, Evidencia B-R).
🚫 Cuándo NO hacer PCI multivaso en shock cardiogénico:
2️⃣ Evitar PCI de arterias no culpables en la fase aguda:
- Aumenta el riesgo de muerte o insuficiencia renal (Clase 3 – Daño, Evidencia B-R).
💡 Puntos clave:
- Revascularización inmediata del vaso culpable es fundamental en shock cardiogénico.
- Evitar PCI de arterias no culpables en la fase aguda.
- Considerar CABG si hay enfermedad multivaso compleja.
Soporte circulatorio mecánico (MCS) en ACS y shock cardiogénico
✅ Cuándo considerar MCS:
1️⃣ En pacientes seleccionados con STEMI y shock cardiogénico severo o refractario:
- Uso de bomba de flujo intravascular (Impella o similar) puede ser razonable para reducir la mortalidad (Clase 2a, Evidencia B-R).
2️⃣ En pacientes con complicación mecánica del ACS (ej. ruptura septal, insuficiencia mitral severa, etc.):
- Dispositivos de MCS a corto plazo pueden ser útiles como puente a cirugía (Clase 2a, Evidencia B-NR).
🚫 Cuándo NO usar MCS:
3️⃣ En pacientes con IAM y shock cardiogénico:
- No se recomienda el uso rutinario de balón de contrapulsación (IABP) o ECMO VA, ya que no mejora la supervivencia (Clase 3 – Sin beneficio, Evidencia B-R).
💡 Puntos clave:
- MCS es útil en casos seleccionados, pero no debe usarse de rutina.
- Impella o dispositivos similares pueden ser considerados en shock refractario.
- IABP y ECMO VA no mejoran la mortalidad de manera rutinaria en estos pacientes.
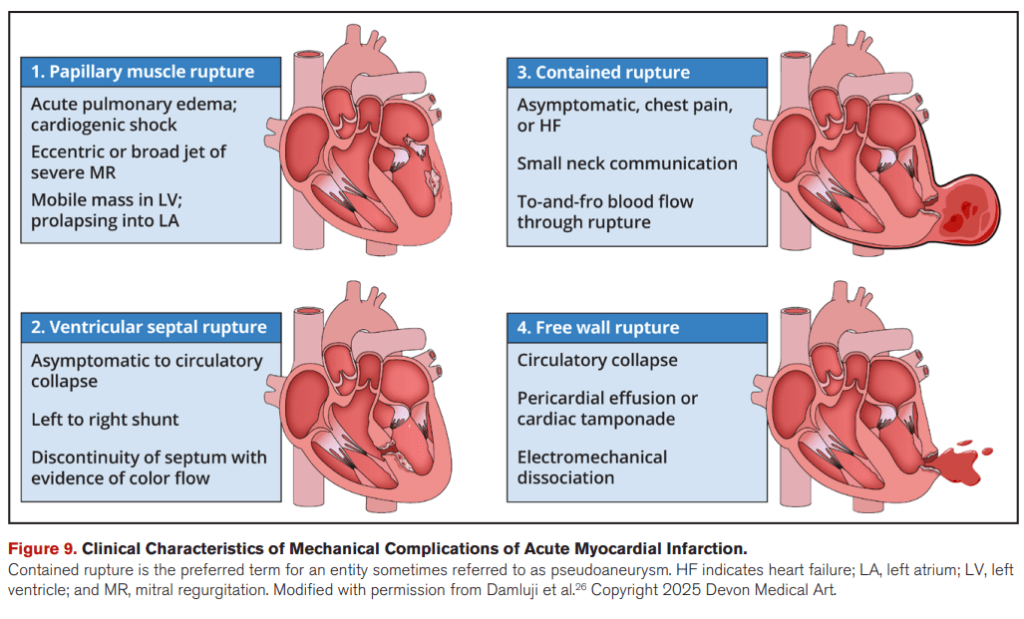
Complicaciones mecánicas del ACS
✅ Manejo recomendado:
1️⃣ Los pacientes con complicaciones mecánicas del ACS (ruptura septal, insuficiencia mitral severa, ruptura de pared libre, etc.)
- Deben ser tratados en centros con cirugía cardiaca disponible (Clase 1, Evidencia C-EO).
2️⃣ Para estabilización hemodinámica antes de cirugía:
- El uso de dispositivos de soporte circulatorio mecánico (MCS) puede ser razonable como puente a cirugía (Clase 2a, Evidencia B-NR).
💡 Puntos clave:
- Requieren manejo en centros con capacidad quirúrgica.
- MCS es una opción para estabilización antes de la cirugía.
- Alto riesgo de mortalidad si no se trata oportunamente.
Complicaciones eléctricas y prevención de muerte súbita tras ACS
✅ Arritmias ventriculares:
1️⃣ Implante de desfibrilador (ICD) post-IAM
- Recomendado en pacientes con FEVI ≤40%, al menos 40 días post-IAM y 90 días post-revascularización, para reducir mortalidad (Clase 1, Evidencia A).
2️⃣ ICD en arritmias ventriculares clínicamente relevantes (>48 h post-IAM):
- Puede ser razonable para mejorar la supervivencia (Clase 2a, Evidencia C-EO).
3️⃣ Uso de desfibrilador portátil temprano en IAM con FEVI <35%:
- Utilidad incierta para mejorar supervivencia (Clase 2b, Evidencia B-R).
✅ Bradiarritmias:
4️⃣ Marcapasos permanente en IAM con bloqueo AV avanzado
- Indicado en IAM con bloqueo AV de segundo grado tipo Mobitz II, bloqueo AV de alto grado, bloqueo de rama alternante o bloqueo AV completo persistente (Clase 1, Evidencia B-NR).
💡 Puntos clave:
- ICD post-IAM en FEVI ≤40% reduce mortalidad.
- Desfibrilador portátil tiene evidencia incierta.
- Marcapasos permanente en bloqueos avanzados post-IAM.
Estrategias de DAPT en los primeros 12 meses post-alta
✅ Duración estándar de DAPT:
1️⃣ En pacientes con ACS sin alto riesgo de sangrado:
- DAPT con aspirina + inhibidor P2Y12 por al menos 1 año para reducir MACE (Clase 1, Evidencia A).
🔹 Estrategias para reducir el riesgo de sangrado:
2️⃣ Suspensión de aspirina y monoterapia con ticagrelor ≥1 mes post-PCI:
- Útil para reducir sangrado en pacientes que toleraron DAPT (Clase 1, Evidencia A).
3️⃣ Uso de IBP en pacientes con alto riesgo de sangrado GI:
- Recomendado si reciben DAPT, anticoagulantes u otros antiplaquetarios (Clase 1, Evidencia A).
4️⃣ De-escalado de DAPT (ticagrelor/prasugrel a clopidogrel) después de 1 mes en PCI:
- Puede ser razonable para reducir riesgo de sangrado (Clase 2b, Evidencia B-R).
5️⃣ Monoterapia (aspirina o P2Y12) después de 1 mes en alto riesgo de sangrado:
- Puede ser considerada para reducir eventos hemorrágicos (Clase 2b, Evidencia B-R).
💡 Puntos clave:
- DAPT ≥1 año en la mayoría de pacientes con ACS.
- Ticagrelor como monoterapia es una opción tras 1 mes en PCI.
- Uso de IBP en alto riesgo de sangrado GI.
- De-escalado o monoterapia puede considerarse en alto riesgo de sangrado.
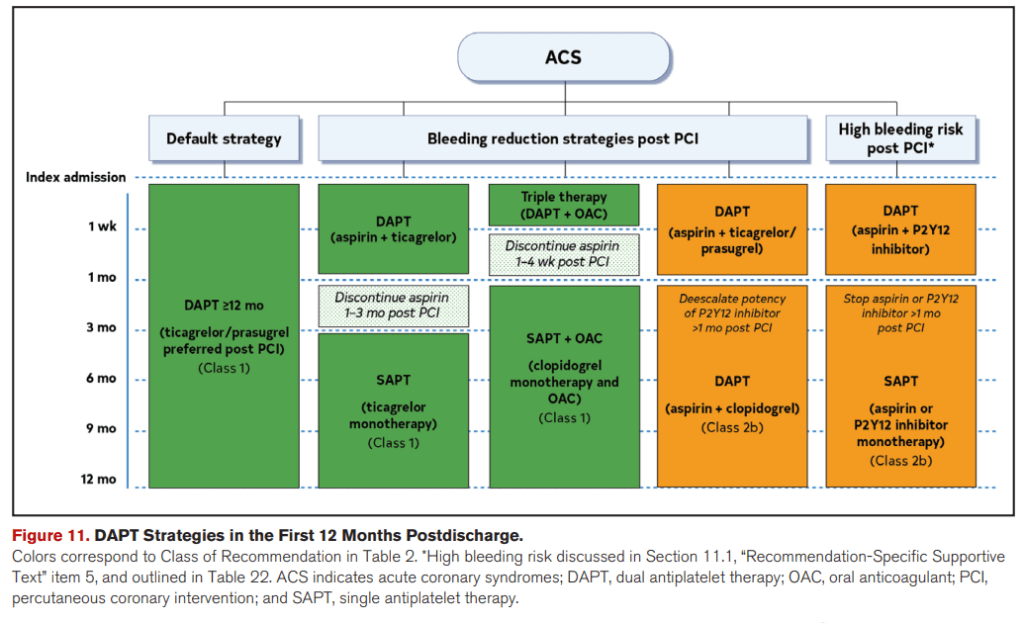
Estrategias de DAPT en los primeros 12 meses post-PCI en ACS
🔹 Estrategia estándar:
✅ DAPT ≥12 meses con ticagrelor o prasugrel + aspirina (Clase 1).
🔹 Estrategias para reducir sangrado:
✅ Triple terapia (DAPT + anticoagulante oral – OAC):
- Suspender aspirina entre 1-4 semanas post-PCI.
✅ SAPT (monoterapia antiplaquetaria):
- Ticagrelor monoterapia desde 3 meses post-PCI (Clase 1).
- Clopidogrel + OAC si requiere anticoagulación (Clase 1).
🔹 Para alto riesgo de sangrado post-PCI:
🔸 Reducción de la intensidad de DAPT:
- Disminuir potencia del inhibidor P2Y12 (>1 mes post-PCI) (Clase 2b).
- DAPT con aspirina + clopidogrel en lugar de ticagrelor/prasugrel (Clase 2b).
🔸 Suspensión de un antiplaquetario:
- Aspirina o P2Y12 después de 1 mes (Clase 2b).
- Monoterapia con aspirina o un inhibidor P2Y12 (Clase 2b).
💡 Puntos clave:
- DAPT ≥12 meses en la mayoría de los pacientes.
- Ticagrelor monoterapia desde los 3 meses es una opción.
- Suspender aspirina en triple terapia con OAC tempranamente.
- Modificaciones en pacientes con alto riesgo de sangrado.
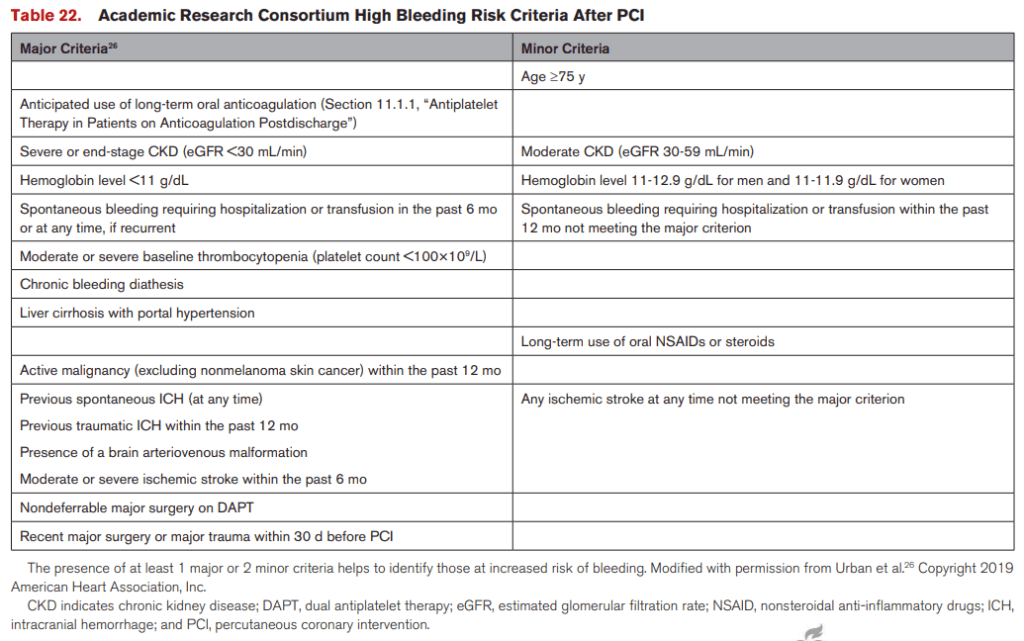
Criterios de alto riesgo de sangrado según el Academic Research Consortium (ARC) después de PCI
🔴 Criterios Mayores:
- Uso anticipado de anticoagulación oral a largo plazo.
- Enfermedad renal crónica (ERC) severa o terminal (eGFR <30 mL/min).
- Hemoglobina <11 g/dL.
- Sangrado espontáneo con hospitalización/transfusión en los últimos 6 meses o recurrente.
- Trombocitopenia moderada o severa (plaquetas <100×10⁹/L).
- Diátesis hemorrágica crónica.
- Cirrosis hepática con hipertensión portal.
- Cáncer activo (excepto carcinoma de piel no melanoma) en los últimos 12 meses.
- ICH espontánea previa (en cualquier momento).
- ICH traumática en los últimos 12 meses.
- Malformación arteriovenosa cerebral.
- Accidente cerebrovascular isquémico severo o moderado en los últimos 6 meses.
- Cirugía mayor no diferible en DAPT.
- Cirugía mayor o trauma grave en los últimos 30 días antes de PCI.
🟡 Criterios Menores:
- Edad ≥75 años.
- ERC moderada (eGFR 30-59 mL/min).
- Hemoglobina 11-12.9 g/dL en hombres, 11-11.9 g/dL en mujeres.
- Sangrado espontáneo con hospitalización/transfusión en los últimos 12 meses sin cumplir criterio mayor.
- Uso crónico de AINEs o esteroides.
- Accidente cerebrovascular isquémico sin cumplir criterio mayor.
💡 Pacientes con ≥1 criterio mayor o ≥2 criterios menores tienen alto riesgo de sangrado.
Terapia antiplaquetaria en pacientes con anticoagulación postalta
✅ Pacientes con ACS que requieren anticoagulación oral:
- Aspirina debe suspenderse entre 1-4 semanas después de la terapia triple inicial.
- Continuar con un inhibidor P2Y12 (preferiblemente clopidogrel) más un anticoagulante oral para reducir el riesgo de sangrado.
💡 Punto clave:
- Se evita la triple terapia prolongada debido al alto riesgo de sangrado.
Reevaluación de los niveles de lípidos postalta
📌 Recomendación:
- En pacientes post-ACS, se recomienda un perfil lipídico en ayunas a las 4-8 semanas tras iniciar o ajustar la terapia hipolipemiante.
- Objetivo: evaluar respuesta y adherencia al tratamiento.
💡 Punto clave:
- Permite ajustes terapéuticos para alcanzar metas de LDL-C.
Uso crónico de colchicina en ACS
📌 Recomendación:
- En pacientes post-ACS, colchicina en dosis bajas puede ser razonable para reducir el riesgo de eventos cardiovasculares mayores (MACE).
🔎 Nivel de evidencia:
- Clase 2b (B-R) → Beneficio potencial, pero con evidencia limitada.
💡 Punto clave:
- Su acción antiinflamatoria podría mejorar el pronóstico cardiovascular.
Inmunización en ACS
📌 Recomendación:
- En pacientes con ACS sin contraindicaciones, se recomienda la vacunación anual contra la influenza para reducir el riesgo de muerte y eventos cardiovasculares mayores (MACE).
🔎 Nivel de evidencia:
- Clase 1 (A) → Evidencia sólida de beneficio.
💡 Punto clave:
- La infección por influenza puede desencadenar eventos cardiovasculares adversos, por lo que la prevención con vacuna es una estrategia eficaz.
Descubre más desde Medicina Cardiometabólica
Suscríbete y recibe las últimas entradas en tu correo electrónico.


Un comentario sobre “Guías ACC/AHA 2025 Manejo de los pacientes con síndromes coronarios agudos”